Галогениды - олово
Cтраница 1
Галогениды олова ( II) и свинца ( II) проявляют свойства солей. [1]
Галогениды олова получают нагреванием олова с га-логеноводородными кислотами НХ; только SnF. SnCb имеют практическое значение. Они легко растворимы в донорных растворителях, таких, как ацетон, этилацетат или пиридин, с образованием непрочных комплексов, обладающих, очевидно, пирамидальной hj - тетраэдрической) структурой ( см. гл. [2]
Галогениды олова получают нагреванием олова с га-логеноводородными кислотами НХ; только SnF, и SnCU имеют практическое значение. Они легко растворимы в доыорных растворителях, таких, как ацетон, этилацетат или пиридин, с образованием непрочных комплексов, обладающих, очевидно, пирамидальной ( j тетраэдрической) структурой ( см. гл. [3]
Известны все галогениды олова в четырехвалентном состоянии. Молекулы SnF4 представляют собой правильные тетраэдры с атомом Sn в центре. [4]
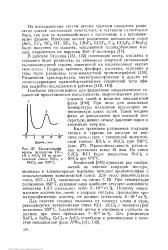 |
Хроматографи-теское разделение TiC l4 ( / и ShCl3 ( 2 на эвтектической смеси BiCl3 и РЬС12 при 240 С. [5] |
В работах Тадмора [131, 132] галогениды олова, мышьяка и германия были разделены на химически инертной силиконовой пысоковакуумпой смазке, нанесенной на изоляционный кирпич силь-о-сель. [6]
Методом ЯКР изучено большое число комплексов, содержащих галогениды олова или их органические производные. [7]
Алкильные соединения олова проявляют значительно меньшую способность к-образованию продуктов присоединения, чем галогениды олова, причем способность к присоединению тем меньше, чем больше атомов галогена замещено на алкилы. [8]
Алкшгьные соединения олова проявляют значительно меньшую способность к-образованию продуктов присоединения, чем галогениды олова, причем способность к присоединению тем меньше, чем больше атомов галогена замещено на алкилы. [9]
Алкильные соединения олова проявляют значительно меньшую способность к образованию продуктов присоединения, чем галогениды олова, причем способность к присоединению тем меньше, чем больше атомов галогена замещено на алкилы. [10]
В газообразном состоянии его молекулы имеют угловую форму ( так же как РЬВг2 и РЫ2; см. галогениды олова ( П), стр. [11]
Исследуя галогениды переходных металлов, Тадмор [42-44] показал, что РеС13 и HgCl2 разделяются при 320 С на чистом трихлориде висмута, являющемся жидкой фазой, а галогениды олова хорошо отделяются друг от друга на силоиеле, покрытом А1Вг3, при 150 С. [13]
Другие металлы дают спектры, состоящие из весьма большого числа густо расположенных линий, заполняющих всю видимую область, как, например, скандий, титан, диспрозий и др. Галогениды олова дают непрерывные молекулярные спектры. [14]
Алкилирование галоидсодержащими соединениями ( при кипячении, с 30 - 80 % - ным выходом) [532] и галоидирование элементарным хлором или бромом ( при 5 - 20 С) [402-406, 533] ароматических соединений до монозамещенных продуктов селективно катализируют свежеосажденные галогениды олова и свинца, хотя к числу самых активных катализаторов указанных процессов они не принадлежат. [15]
Страницы: 1 2