Галогениды - таллий
Cтраница 2
Таллий и его соединения имеют небольшое по объему, но разнообразное применение. Галогениды таллия хорошо пропускают инфракрасные лучи. Поэтому они используются в оптических приборах, работающих в инфракрасной области спектра. Карбонат таллия служит для изготовления стекол с высокой преломляющей способностью. Таллий входит в состав вещества электрода селенового выпрямителя, является активатором многих люминофоров. Сульфид таллия используется в фотоэлементах. [16]
Таллий и его соединения имеют небольшое по объему, но разнообразное применение. Галогениды таллия хорошо пропускают инфракрасные лучи. Поэтому они используются в оптических приборах, работающих в инфракрасной области спектра. Карбонат галлия служит для изготовления стекол с высокой преломляющей способностью. Таллий входит в состав вещества электрода селе-нового выпрямителя, является активатором многих люминофоров. Сульфид таллия используется в фотоэлементах. [17]
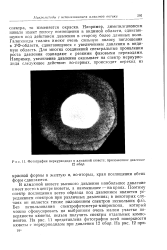 |
Фотография меркуриодида в алмазной кювете. приложенное давление. [18] |
Например, диметилглиоксим никеля имеет полосу поглощения в видимой области, сдвигающуюся под действием давления в сторону более длинных волн. Галогениды таллия имеют очень сильную полосу поглощения в УФ-области, сдвигающуюся с увеличением давления в видимую область. Для многих соединений спектральные проявления роста давления совпадают с резкими фазовыми переходами. [19]
Таллий и его соединения имеют небольшое по объему, но разнообразное применение. Галогениды таллия хорошо пропускают инфракрасные лучи. Поэтому они используются в оптических приборах, работающих в инфракрасной области спектра. Карбонат таллия служит для изготовления стекол с высокой преломляющей способностью. Таллий входит в состав вещества электрода селенового выпрямителя, является активатором многих люминофоров. Сульфид таллия используется в фотоэлементах. [20]
Талл:: м и его соединения имеют небольшое по объему, но разнообразное применение. Галогениды таллия хорошо пропускают инфракрасные лучи. Поэтому они используются в оптических приборах, работающих в инфракрасной области спектра. Карбонат таллия служит для изготовления стекол с высокой преломляющей способностью. Таллий входит в состав вещества электрода селенового выпрямителя, является активатором многих люминофоров. Сульфид таллия используется в фотоэлементах. [21]
Галогениды таллия удивительно сходны с галогенидами серебра ( I) и по цвету, и по растворимости, хотя они имеют различную кристаллическую структуру вследствие различий в размерах и степени поляризуемости катионов. AgF, растворим в воде, тогда как другие галогениды очень малорастворимы. [22]
Таллий и его соединения имеют небольшое по объему, но разнообразное применение. Галогениды таллия хорошо пропускают инфракрасные лучи. Поэтому они используются в оптических приборах, работающих в инфракрасной области спектра. Карбонат таллия служит для изготовления стекол с высокой преломляющей способностью. Таллий входит в состав вещества электрода селенового выпрямителя, является активатором многих люминофоров. Сульфид таллия используется в фотоэлементах. [23]
Таллий и его соединения имеют небольшое по объему, но разнообразное применение. Галогениды таллия хорошо пропускают инфракрасные лучи. Поэтому они используются в оптических приборах, работающих в инфракрасной области спектра. Карбонат галлия служит для изготовления стекол с высокой преломляющей способностью. Таллий входит в состав вещества электрода селенового выпрямителя, является активатором многих люминофоров. Сульфид таллия используется в фотоэлементах. [24]
Эти галогениды таллия получают осаждением из сульфатных или нитратных растворов. После удаления осадка, который может образоваться при наличии примесей в растворе, последний упаривают до появления пленки и добавляют к нему кристаллический хлористый аммоний. Полученные галогениды сплавляют и подвергают кристаллофизической очистке зонной плавкой или направленной кристаллизацией, после чего из чистой соли выращивают монокристаллы. [25]
Таллийоргани-ческие соединения этого типа плохо растворимы в эфире и выделяются в виде хлопьев уже в самом начале прибавления гриньярова реактива. Для отделения от Т1С1 лучше всего растворять их в горячем пиридине, в котором галогенид таллия не растворим. При охлаждений фильтрата галоидные диалкилталлиевые соединения кристаллизуются в чистом виде. Они отсасываются, промываются эфиром и высушиваются. [26]
Это установлено в лаборатории микроанализа ИНЭОС АН СССР на примере анализа циклопентадиенилталлия. Как выяснено работами Гельман и Шевелевой [ 86а ], элементарный анализ соединений типа RTlHal2 и RaTlHal затруднен летучестью галогенидов одновалентного таллия. Для того чтобы задержать галогениды таллия в трубке для сожжения, рекомендуется охладить льдом часть трубки длиной 6 - 8 см, находящуюся между зоной сожжения и окислительной зоной. Кроме того, в тех случаях, когда в веществе содержится больше галоида, чем нужно для образования галогенида одновалентного таллия ( для соединений типа, например, RTlHal2), необходимо помещать между окислительной зоной и охлажденной частью трубки нагретое серебро для улавливания галоида. Даже принятие таких мер предосторожности не всегда позволяет избежать уноса галогенидов таллия из трубки для сожжения. Описанным способом были получены удовлетворительные результаты для ряда галоидсодержащих таллийорганических соединений с непредельными и ароматическими радикалами. [27]
Соединения таллия очень ядовиты Соединения таллия ( I) устойчивее соединений таллия ( III); соединения таллия ( I) сходны по свойствам с соединениями щелочных элементов, серебра и свинца. Оксид таллия ( 1) ТЬО - черное вещество, реагирующее, с водой с образованием бесцветного раствора щелочи - гидроксида таллия ( 1) Т10Н, который в твердом состоянии имеет желтую окраску. Карбонат таллия () Т12СО3 хорошо растворим в воде; раствор ТЬСОз вследствие гидролиза сильнощелочной. Галогениды таллия ( 1) различаются по растворимости в воде; T1F хорошо растворим, а Т1С1, TIBr и ТП - малорастворимы. Таллий и его соединения обнаруживают по зеленому окрашиванию пламени горелки. [28]
В этой структуре АХ ( рис. 6.5) каждый атом ( ион) окружен восемью равноудаленными ближайшими соседями по вершинам координационного полиэдра - куба. По сравнению со структурой типа NaCl эта структура встречается реже. Она характерна для некоторых интерметаллических соединений, например упорядоченной р-латуни ( CuZn), и таких фаз, как FeAl, TISb, LiHg, LiTl и MgTl, но не встречается ни у каких соединений внедрения МС, MN или МО. Только 3 из галогенидов щелочных металлов и галогениды таллия ( Т1С1, TIBr и ТП) при обычных температурах и давлениях обладают структурой типа CsCl, хотя некоторые галогениды К и Rb переходят в нее под давлением. [29]
Склонность к переходу в одновалентное состояние убывает в ряду Т1 In Ga А1, и химия таллия - это в основном химия однозарядного положительного иона. Ион Т1 очень похож на ионы щелочных металлов тем, что он дает растворимые окись, карбонат, цианид и гидроокись. Нитрат, сульфат и перхлорат изоморфны с соответствующими солями калия. Однако бромат, иодат, сульфид и галогениды закисного таллия ( за исключением фторида) плохо растворимы в воде. Такое поведение сходно скорее с поведением солей Ag, чем солей щелочных металлов. [30]
Страницы: 1 2 3