Галогенирование - ароматические углеводород
Cтраница 1
Галогенирование ароматических углеводородов в присутствии кислот Льюиса отличается тем, что вступающий атом галогена лишь незначительно дезактивирует ароматическое ядро к последующей электрофильной атаке. В частности, хлорирование хлорбензола в присутствии кислот Льюиса ведет к побочному образованию смеси орто - и пара-дихлорбензолов, а также 1 2 4-трихлорбензола. [1]
Галогенирование ароматических углеводородов в присутствии кислот Льюиса отличается тем, что вступающий атом галогена лишь незначительно дезактивирует ароматическое ядро для последующей электрофильнои атаки. В частности, при хлорировании бензола в присутствии кислот Льюиса побочно получают о - и и-дихлорбензолы, а также 1 2 4-трихлорбензол. Продукты полигалогенирования образуются в большей степени, если в качестве катализатора применяют галогениды алюминия. [2]
Галогенирование ароматических углеводородов имеет определенное значение для производства ряда диэлектриков, ядохимикатов, мономеров, разнообразного сырья для производства красителей. [3]
Галогенирование ароматических углеводородов может протекать весьма разнообразно в зависимости от их характера, условий процесса и свойств галогена. Скорость реакции, как и в предыдущих случаях, падает от фтора к иоду. [4]
Реакция галогенирования ароматических углеводородов осуществляется на свету или в присутствии катализаторов. [5]
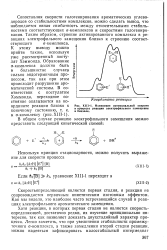 |
Изменение потенциальной энергии в процессе реакции электрофильного замещения в бензоле. [6] |
Сопоставляя скорости галогенирования ароматических углеводородов со стабильностями комплексов, можно сделать вывод, что наблюдается явная симбатность между относительными стабильностями соответствующих а-комплексов и скоростями галогенирования. Таким образом, строение активированного комплекса в реакциях электрофильного замещения близко к строению соответствующего сг-комплекса. [7]
Этот раздел заканчивается рассмотрением галогенирования ароматических углеводородов, фенолов, анилинов, некоторых гетеро-циклов и соединений с электроноакцепторными группами. [8]
В зависимости от условий галогенирования процесс протекает по разным механизмам. Так, галогенирование ароматических углеводородов в присутствии галогенидов железа, алюминия, сурьмы, способствующих образованию галоген-катиона, протекает по элек-трофильному механизму замещения. [9]
По-видимсму, это является следствием большей нуклеофильности этих сседйнений и меньшей способности ртути подвергаться нуклеофильной кссрдинации. Естественно, что при переходе от C6H5HgBr к ( CeH6) 2Hg роль нуклесфильного содействия должна уменьшиться и основным фактором в реакции должна стать электрофильная атака на атсм углерода. Это сближает рассматриваемую реакцию с реакцией галогенирования обычных ароматических углеводородов. [10]
Фтор реагирует с большинством органических веществ со взрывом, поэтому для получения фторпроизводных используют не прямое фторирование, а косвенные способы. С иодом прямое замещение не протекает из-за энергетических затруднений. Для галогенирования алифатических углеводородов необходимо активирование процесса мощным источником света, а для галогенирования ароматических углеводородов - ускорение с использованием катализаторов. [11]
Страницы: 1