Галогенофторид
Cтраница 1
Галогенофториды пятивалентного ф о с фо р а получаются присоединением галогенов к соответствующим соединениям трехвалентного фосфора. Плотность газа близка к теоретической. Дихлортрифторид фосфора бесцветен, обладает резким раздражающим запахом, дымит на воздухе. [1]
Так как эти галогенофториды во фтористоводородной системе являются основаниями, сам фтористый водород в такой системе проявляет кислотные свойства. [2]
Очень хороший метод синтеза смешанных галогенофторидов основан на взаимодействии фторида металла или неметалла с соответствующим хлоридом, бромидом или иодидом. Эту методику широко применяли в химии кремния. [3]
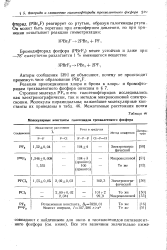 |
Молекулярные константы галогенидов трехвалентного фосфора. [4] |
Строение молекул PF3 и его галогенофторидов исследовалось как электронографически, так и методом микроволновой спектроскопии. [5]
Вместо свободного фтора часто можно использовать галогенофториды, для получения которых, однако, также необходим свобод-шый фтор. Неудобство применения галогенофторидов как фторирующих агентов состоит в трудности отделения продукта реакции от образующегося в результате фторирования свободного галогена. [6]
При подобных условиях трихлорид фосфора дает смесь галогенофторидов. [7]
Подобно тому, как это наблюдалось для галогенофторидов трехвалентного фосфора, температуры кипения и теплоты испарения веществ существенно возрастают при замещении атомов фтора на атомы хлора и, особенно, брома. [8]
Вместо свободного фтора часто можно использовать галогенофториды, для получения которых, однако, также необходим свобод-шый фтор. Неудобство применения галогенофторидов как фторирующих агентов состоит в трудности отделения продукта реакции от образующегося в результате фторирования свободного галогена. [9]
В пятифтористых фосфоре и мышьяке происходит гибридизация dsps электронов и соответственно этому молекулы этих веществ имеют форму тригональной бипирамиды. Вероятно, такова же форма многочисленных галогенофторидов пятивалентного фосфора; различие размеров атомов фтора и других галогенов и меньшая прочность связи последних может привести к искажению бипирамиды. Вопрос о существовании галогенофторидой пятивалентной сурьмы не разрешен окончательно. [10]
Соединения фтора с кремнием значительно менее многочисленны, чем соединения его с углеродом. Помимо SiF4, известны Si2F6, продукты неполного замещения водорода силана на фтор, различные галогенофториды кремния и ряд содержащих кремне-кислородные цепи фторсилокеанов. [11]
Галогенофторосиланы значительно менее устойчивы, чем соответствующие соединения углерода. Аналогичные соединения германия легко подвергаются реакциям симметризации; вопрос о существовании подобных соединений олова не решен окончательно. Известны галогенофториды двухвалентного свинца. [12]
Лишь несколько гало-генидов не вступают в обменную реакцию с фторидом сурьмы. Судя по накопленному опыту, основная характерная черта этого реагента заключается в том, что многие обменные реакции приводят к образованию суспензий и смесей фторидов, и часто образуются галогенофториды. [13]
Вместо свободного фтора часто можно использовать галогенофториды, для получения которых, однако, также необходим свобод-шый фтор. Неудобство применения галогенофторидов как фторирующих агентов состоит в трудности отделения продукта реакции от образующегося в результате фторирования свободного галогена. Галогенофториды как фторирующие агенты обладают различной активностью, например: С1Р3 сравнительно активен, IF5 - мягкий фторирующий агент. [14]
Страницы: 1