Гальванопара
Cтраница 4
Итак, какой процесс будет протекать при работе гальванопары, зависит от рН: в кислой среде выделяется водород, в нейтральной и щелочной средах ( при коррозии стали, железа) происходит кислородная деполяризация катода и водород не выделяется. [46]
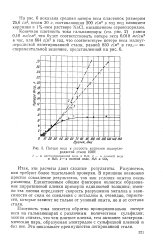 |
Потеря веса и скорость коррозии. малоуглеродистой стали 1020. [47] |
Плотность тока меняется обратно пропорционально потере веса на гальванопарах с различным количеством сульфидов; можно считать, что чем плотнее пленка, тем активнее электрохимическая пара, образуемая электродом с сульфидной пленкой и без нее. Это показывает преимущество легированной стали. [48]
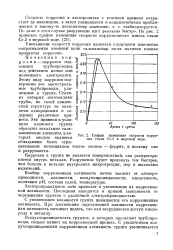 |
График изменения скорости коррозии стали Ст. З в морской воде. [49] |
Уменьшение скорости коррозии является следствием изменения сопротивления внешней цепи гальванопар из-за наличия пленки продуктов коррозии. [50]
Наличие сульфидов железа в составе осадка приводит к возникновению гальванопары Fe-FeS, интенсифицирующей процесс локализации коррозии. [51]
Выше было высказано обоснование предположение, что сила коррозионного тока гальванопары СОП - старая поверхность является инвариантной характеристикой раэупрочняющего воздействия среды на скачкообразном ( водородно-механичес-ком) этапе развития трещины. [52]
Химически чистое железо, в котором отсутствуют условия для появления поверхностных гальванопар, не подвержено электрохимической коррозии. Однако углеродистые и даже слаболегированные стали, используемые в энергетике, вне зависимости от структуры и содержания примесей практически в одинаковой степени страдают от кислородной и углекислотнои коррозии. Данное обстоятельство позволяет на практике без особой погрешности использовать для индикаторов коррозии сталь, по химическому составу и структуре не идентичную металлу контролируемой поверхности. Это объясняется влиянием меди на плотность защитных оксидных пленок. [53]
Помимо пар дифференциальной аэрации, вызванных краевым эффектом, могут образовываться гальванопары между отдельными точками края резервуара. [54]
Электродный потенциал никеля более положительный, чем железа, поэтому в гальванопаре с железом он будет служить катодом, ускоряя коррозию железа. Таким образом, никелевые покрытия будут защищать железо только механически, в случае отсутствия пор в покрытии. [55]
Выше отмечалось, что электрохимическая коррозия металлов характеризуется работой короткозамкнутых гальваноэлементов ( гальванопар), возникающих на поверхности металла при взаимодействии его с электролитом. При этом на поверхности металла возникает множество анодных и катодных участков. Под влиянием разности потенциалов отдельных электродов возникает коррозионный ток. [56]
Если t if1, Периоды работы, как первой, так и второй гальванопары, частично накладываются друг на друга, только пики их интенсивной деятельности не совпадают во времени. [57]
Страницы: 1 2 3 4