Гидроксиль-ной ион
Cтраница 4
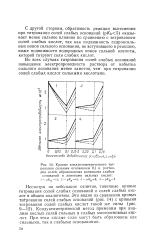 |
Кривые кондуктометрического титрования сильным основанием 0 1 н. растворов солей, образованных катионами слабых оснований и анионами сильных кислот. [46] |
С другой стороны, обратимость реакции вытеснения при титровании солей слабых оснований ( р / Сь5) оказывает менее сильное влияние по сравнению с титрованием солей слабых кислот, так как подвижность гидроксиль-ных ионов сильного основания, не вступившего в реакцию, ниже подвижности водородных ионов сильной кислоты, которой титруют соли слабых кислот. [47]
 |
Схема образования бугристых коррозийных отложений. [48] |
Сначала на анодных участках образуются язвины, развивающиеся в глубь металла, которые заполняются осадком гидрата закиси железа в результате реакции между переходящими в раствор ионами железа и образующимися на катодных участках гидроксиль-ными ионами. Рыхлый осадок гидрата закиси железа имеет объем, в несколько раз больший первоначального объема металла, и вследствие этого образуется бугорок. На поверхности бугорка гидрат закиси железа окисляется растворенным в воде кислородом, в результате чего бугорок покрывается слоем гидрата окиси железа красноватого или коричневого цвета. Так как гидраты окиси и закиси железа имеют некоторую пористость, то коррозия в данном случае не прекращается. [49]
При реакции нейтрализации исчезают свойства основания и кислоты, несмотря на то, что ионы металла и кислотного остатка, как это видно из схемы, остаются в растворе без изменения, а связываются лишь ионы водорода и гидроксиль-ные ионы. Это подтверждает, что носителями основных свойств являются гидроксильные ионы, а носителями кислотных свойств - ионы водорода. Реакция нейтрализации, таким образом, вне зависимости от взятых основания и кислоты, сводится к тому, что гидроксильные ионы образуют с ионами водорода мало диссоциированные молекулы воды. [50]
В р-рах кислот и щелочей Сн не будет равно Сон, но в любом случае, как видно из уравнения ( 16), будет сохраняться обратная пропорциональность между этими величинами и, следовательно, любое повышение концентрации водородных ионов вызовет соответствующее уменьшение концентрации гидроксиль-ных ионов, и наоборот. [51]
Страницы: 1 2 3 4