Обмениваемый ион
Cтраница 2
В зависимости от знака заряда обмениваемых ионов ( катионов или анионов) ионообыенники подразделяют на катиониты п аниониты. Очевидно, что для умягчения воды применяют катиониты. [16]
Константа обмена является мерой сродства обмениваемого иона к решетке обменника. [17]
В зависимости от знака заряда обмениваемых ионов ( катионов или анионов) ионообменники подразделяют на катиониты и аниониты. Очевидно, что для умягчения воды применяют катиониты. [18]
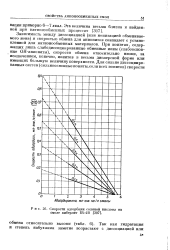 |
Скорости адсорбции соляной кислоты на смоле амберлит IR - 4B. [19] |
Зависимость между диссоциацией ( или ионизацией обмениваемого иона) и скоростью обмена для анионитов совпадает с установленной для катионообменных материалов. При ионитах, содержащих лишь слабодиссоциированные обменные ионы ( слабоосновные ОН-ашгониты), скорости обмена относительно низки, за исключением, конечно, ионитов в весьма дисперсной форме или имеющих большую величину поверхности. [20]
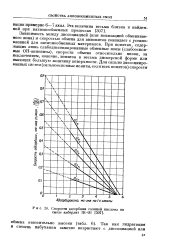 |
Скорости адсорбции соляной кислоты на смоле амберлит Ш-4 В. [21] |
Зависимость между диссоциацией ( или ионизацией обмениваемого иона) и скоростью обмена для анионитов совпадает с установленной для катионообменных материалов. При ионитах, содержащих лшпь слабодиссоциированные обменные ионы ( слабоосновные ОН-аниониты), скорости обмена относительно низки, за исключением, конечно, ионитов в весьма дисперсной форме или имеющих большую величину поверхности. [22]
Емкость смолы обычно выражается в миллиэквива-лентах обмениваемого иона на 1 г смолы. Выпускаемые промышленностью катионообменные смолы содержат примерно одну функциональную группу на одно бензольное кольцо и имеют емкость обмена около 4 5 мэкв. [23]
Аналогично пусть Sn r - доля обмениваемого иона в смоле на той же тарелке. [24]
Обычно обменная емкость ионитов выражается в мг-экв обмениваемых ионов на 1 г сухого ионита. [25]
В первых двух стадиях эквивалентные количества обменивающихся и обмениваемых ионов движутся друг к другу, за исключением небольшого отрицательного потока, связанного с изменениями содержания электролита в обменнике. Если некоторые из ионов в растворе образуют комплекс, то кинетика образования или диссоциация этого комплекса может составить дополнительную стадию во всем кинетическом процессе. [26]
 |
Кажущиеся константы диссоциации характерных ионогенных групп ионообменников ( рК - I. [27] |
Каждый ионообменник содержит определенное число групп с подвижными обмениваемыми ионами. Число таких групп в единице массы ( объема) ионообменника характеризует величину обменной емкости, которая теоретически может быть выражена в произвольно выбранных единицах. В области ионообменников строгой терминологии до сих пор не установлено. [28]
Причиной изменения осмотического давления является перенос растворителя вместе с обмениваемыми ионами из одной фазы в другую и обратно. Так, при переходе иона А из внешнего раствора в ионообменник ( Ао - A) / молей растворителя переносится из 0-фазы в / - фазу. Одновременно при переходе иона В из ионообменника во внешний раствор ( Bt - B q молей растворителя переносится из г - фазы в 0-фазу. [29]
Обменная емкость по однотипным группам, соответствующая предельному насыщению обмениваемыми ионами активных групп одного типа ( при наличии в ионите групп и других типов), также является постоянной величиной. Для определения обменной емкости ионитов существует два основных метода: статический и динамический. [30]
Страницы: 1 2 3 4