Обменивающийся ион
Cтраница 1
Обменивающиеся ионы называются противоионами, а ионы, образованные диссоциированными функциональными группами и связанные химической связью с углеродными атомами молекулярных цепей матрицы смолы, называются фиксированными. [1]
Если обменивающиеся ионы имеют одинаковые заряды, то размерность коэффициента селективности не зависит от единиц измерения концентрации в растворе и в ионите, тогда как при различных значениях зарядов ионов численное значение коэффициента селективности зависит от единиц измерения концентрации. [2]
Подвижные обменивающиеся ионы проникают через поверхность ионита в обоих направлениях, а высокомолекулярные ионы с противоположным зарядом, из которых состоит основная масса ионита, неподвижны. [3]
Концентрация обменивающихся ионов в растворе выражается обычно в единицах молярности или моляльности. [4]
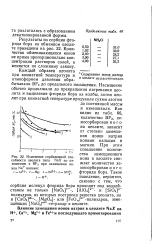 |
Изменение сорбционной способности цеолита типа NaX по отношению к ВРз при замещении ионов Na. ионами. / Са2. 2 - Mg. 3 - Fe3. 4 - NH. [5] |
Количество обменивающихся ионов не прямо пропорционально концентрации растворов солей, а меняется по сложному закону. [6]
С - обменивающиеся ионы ( заряды опущены), а индексы с и р соответственно обозначают смолу и раствор. [7]
Физико-химические свойства обменивающихся ионов ( радиус, объем, степень гидратации) имеют в процессе ионообмена не менее важное значение, чем рН среды. [8]
Степень сродства обменивающихся ионов к иониту уменьшается с увеличением радиуса гидратированных ионов и возрастает по мере увеличения валентности ионов. При этом в отдельных случаях немалую роль играет химическое сродство отдельных ионов к активным группам ионита, а также взаимодействие ионов по мере увеличения концентрации растворов. [9]
Если заряды обменивающихся ионов одинаковы, константа, выражаемая уравнением (111.149), соответствует коэффициенту разделения. [10]
Коэффициенты диффузии обменивающихся ионов могут значительно различаться. Например, экспериментально установлено, что когда процесс лимитируется внутренней диффузией, обмен между Н - катионитом и находящимся в растворе ионом металла идет быстрее, чем между Ме-катионитом и ионом водорода, коэффициент диффузии которого больше, чем иона металла. Но при этом, несмотря на различие коэффициентов диффузии отдельных ионов, в макроскопических масштабах разделения зарядов при ионном обмене не происходит, электрические поля ионов влияют на их взаимное перемещение, система и в жидкой, и в твердой фазах остается электронейтральной, а скорость процесса определяется скоростью взаимной диффузии ионов. [11]
Характер распределения обменивающихся ионов в составе раствора ( жидкая фаза) ионита ( твердая фаза) определяется величинами констант обмена между этими ионами. [12]
Количественное поглощение обменивающихся ионов достигается даже при таких малых концентрациях, как 10 - 5 - 10 6 моль; 3) применимость для разделения смесей веществ, очень близких по составу, строению и свойствам; 4) высокая степень разделения, значительно выше, чем методов дробной кристаллизации и перегонки; 5) простота выполнения и аппаратуры. [13]
По знаку заряда обменивающихся ионов иониты делят на кати-ониты и аниониты, проявляющие соответственно кислотные и основные свойства. Практическое значение имеют неорганические природные и искусственные алюмосиликаты, гидроокиси и соли многовалентных металлов; применяются также иониты, полученные химической обработкой угля, целлюлозы и лигнина. [14]
Количественная оценка распределения обменивающихся ионов между раствором и смолой значительно упрощается при использовании радиоактивных изотопов в индикаторных количествах. [15]
Страницы: 1 2 3 4