Активация - титан
Cтраница 1
 |
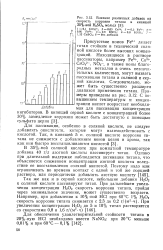
Изменение во времени потенциалов титана ВТ1 - 0 ( 1, сплавов 4207 ( 2 и 4200 ( 3 в растворе 25 % - ного Ш4С1 2 % - ная НС1 при 100 С. [1] |
Активация титана наступает при введении в эти растворы соляной или бромистоводородной кислоты. [2]
Такой ряд должен свидетельствовать об активации титана сульфатом аммония. Такое изменение реакционной способности свидетельствует об активирующем действии натрия. [3]
 |
Пороги коррозионной устойчивости титана BTI-0 в подкисленных насыщенных растворах хлоридов. [4] |
Так, если в растворах ZnCl2 активация титана в зависимости от содержания кислоты происходит через 10 - 60 мин, то в растворах MgCl. [5]
 |
Скорость коррозии [ г / ( ж2 - ч ] титана в растворах 40 % - ной H2SOi Ti ( IV-uonbi при, 60 С. [6] |
Следует обратить внимание на близость Е реакции (2.52) и потенциалов активации пассивного титана или Епп, тогда как стандартные потенциалы реакций, рассматриваемых обычно при пассивации титана ( см. табл. 2.1 и 2.2), имеют гораздо более отрицательные значения. Адсорбция Ti ( IV) - ионов на наиболее активных участках поверхности титана с последующим участием в реакции образования пассивной пленки приводит к формированию более совершенной, менее дефектной пленки. Можно полагать, что Ti ( IV) - ионы способствуют ого-меризации пассивной пленки. [7]
Диапазон пассивного состояния титана очень широк, и в обычных условиях не наблюдается активация титана в окислительных средах ионами хлора. Поэтому титан устойчив, главным образом, к воздействию окислительных сред. В восстановительных средах, в которых окиснаа шшнка растворяется, он обладает незначительной стойкостью. [8]
На основе [33, 34] можно считать установленным, что в катодный импульс тока происходит активация титана вследствие восстановления пассивирующего слоя кислорода. В следующий анодный цикл наряду с реакцией ионизации металла протекает адсорбция кислорода. Другими словами, коррозия титана за отдельный импульс является параболической функцией длительности анодного цикла. Однако необходимо заметить, что подобные представления допустимы при двух условиях: во-первых, образование поверхностного слоя кислорода происходит мгновенно, и, следовательно, в измеряемую величину коррозии не входят потери металла за время завершения адсорбции первого слоя кислорода, во-вторых, на поверхности металла возникает более чем мономолекулярный слой кислорода. Разумеется, допущение о мгновенной адсорбции кислорода с учетом известной зависимости скорости адсорбции частиц от времени [43] не может быть принято. Можно лишь предполагать, что вследствие медленного процесса перезаряжения двойного электрического слоя после изменения полярности тока необходимый анодный потенциал электрода достигается недостаточно быстро. [9]
Наблюдается определенная зависимость между активностью воды исходного раствора и критическим количеством НС1, необходимой для активации титана. [10]
Поэтому ничтожная добавка НС1 ( 0 02 %) к 40 % - ному LiCl приводит к изменению рН от 5 6 до - 0 1 и вызывает активацию титана. В этой связи примечателен также тот факт, что какой-либо зависимости порогов стойкости титана от рН при переходе от одного раствора хлорида к другому не наблюдается. [12]
Поэтому ничтожная добавка соляной кислоты ( 0 02 %) к 40 % раствору хлористого лития приводит к изменению рН от 5 6 до - 0 1 и вызывает активацию титана. В этой связи примечателен также тот факт, что какой-либо зависимости порогов стойкости титана от значений рН при переходе от одного раствора хлорида к другому не наблюдается. [13]
Если при добавлении 5 г / л SO2 в раствор 200 г / л H2SO4 при 60 С коррозия титана предотвращается, то в этом случае контакт титана с активно-растворяющейся нержавеющей сталью 12Х18Н10Т приводит к катодной поляризации и активации титана. [14]
 |
Влияние различных добавок на скорость коррозии титана в кипящей 30 % - ной H2S04, моль / л. [15] |
Страницы: 1 2
