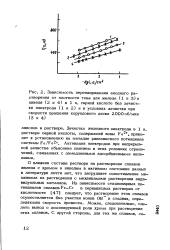
Активация - электрод
Cтраница 1
Активация электродов при непрерывной зачистке объяснена снятием в этих условиях ограничений, связанных с замедленными адсорбционными явлениями. [2]
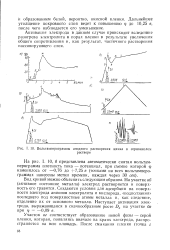 |
Вольтамперограммы анодного растворения цинка в сернокислом. [3] |
Активация электрода в данном случае происходит вследствие разогрева электролита в порах пленки в результате увеличения общего сопротивления и, как результат, частичного растворения пассивирующего слоя. [4]
Активацию электрода обычно начинают с анодной поляризации, а заканчивают тоже анодной, если на платине предполагается. Можно заканчивать активацию и при потенциале около 0 5 в ( НВЭ) независимо от того, будут ли на электроде протекать реакции восстановления или окисления. При работе с таким электродом необходимо иметь в виду, что его активность со временем постепенно уменьшается. По данным Френча и Куваны7, время, в течение которого активность электрода уменьшается в два раза, составляет около 45 мин. Поэтому для поддержания активного состояния поверхности электрода его следует периодически подвергать анодно-катодной поляризации. [5]
Активацию электрода обычно начинают с анодной поляризации, а заканчивают тоже анодной, если на платине предполагается проведение процессов восстановления, или катодной, если электрод будет использован для процессов окисления. Можно заканчивать активацию и при потенциале около 0 5 в ( НВЭ) независимо от того, будут ли на электроде протекать реакции восстановления или окисления. При работе с таким электродом необходимо иметь в виду, что его активность со временем постепенно уменьшается. Поэтому для поддержания активного состояния поверхности электрода его следует периодически подвергать анодно-катодной поляризации. [6]
При активации электрода № 0 - 1 алюминий вообще не растворялся. Это можно объяснить особыми условиями изготовления электрода ( разд. Такие электроды, конечно, непригодны в качестве водородных электродов, так как их электрохимическая активность определяется лишь структурой спеченного из никеля пористого тела и поэтому при рабочих температурах от 20 до 80 С низка. При 40 С даже не устанавливается водородный потенциал. [7]
При активации электрода алюминий из сплава растворяется, но при этом механическая прочность электрода сохраняется, поскольку имеется спеченный каркас ( скелет) из карбонильного никеля, вторым скелетом служит никель Ренея с неупорядоченной структурой. Анодная поляризация позволяет ускорить растворение алюминия. [8]
При активации электрода алюмкний из сплава растворяется, но при этом механическая прочность электрода сохраняется, поскольку имеется спеченный каркас ( скелет) из к. НИЛЬНбТо Никеля, вторым скелетом служит никель Ренея с неупорядоченной структурой. Анодная поляризация позволяет ускорить растворение алюминия. [9]
Возрастание тока, соответствующее активации электрода, происходит при некотором критическом значении потенциала ркр. [10]
Взаимоотношение скоростей пассивации и активации электрода определяет не только перенапряжение палладия, но также и величину его активной поверхности. Последняя, в свою очередь, обусловливает величину предельного тока диффузии преобладающих в электролите ионов, из которых происходит выделение металла. [11]
В низкотемпературных ТЭ для активации электродов используются катализаторы, в основном дорогие и дефицитные материалы. [12]
Некоторые технические решения предусматривают также активацию электрода из золота с помощью тока деполяризации, протекающего между этим электродом и добавочным платиновым электродом. Встречаются также и измерители, соединенные с датчиком, состоящие из каломелевого и платинового электродов. [13]
Для снижения перенапряжения водорода были предложены различные способы так называемой активации электродов путем нанесения на их поверхность электролитически различных металлов ( молибдена, вольфрама, ванадия) или сплавов. Эффект, обусловленный активацией электродов, сохраняется в течение длительного времени только при условии тщательной очистки электролита от примесей солей железа. В этом случае катоды, активированные никелевым покрытием, содержащим серу, обеспечивают снижение напряжения на ячейке на 2 % в течение двух лет. [14]
Разработанный радиохимический метод определения малых скоростей растворения металлов основан на предварительной нейтральной активации электродов в ядерном реакторе и определении скорости перехода образующихся при этом радиоизотопов в раствор в условиях испытания путем периодического отбора проб электролита и анализа их с помощью многоканальных сцинтилляционных гамма-спектрометров. Применение гамма-спектрометров обеспечивает высокую чувствительность, селективность измерений и в ряде случаев позволяет определять парциальные скорости растворения компонентов сложных сплавов. [15]
Страницы: 1 2 3 4