Сольва-тированный ион
Cтраница 1
Сольва-тированные ионы имеют сравнительно большой размер, и поэтому у них расстояние максимального сближения гораздо больше, чем у голых несольватированных ионов. [1]
Понятие ионной пары было введено Бьеррумом для сольва-тированных ионов, находящихся на близком расстоянии друг от друга в растворе. В последние годы было показано, что ионная пара обладает большей стабильностью, чем это следует из модели Бьеррума. Простейшей моделью для контактной ионной пары, которая согласуется с этими данными, является модель двухатомной частицы Na A - в клетке растворителя. [2]
Первый член в этом уравнении представляет энергию переноса сольва-тированных ионов с радиусом ги из вакуума в среду М с диэлектрической проницаемостью е по Борну. [3]
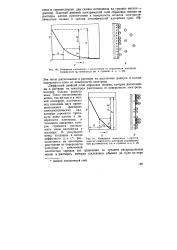 |
Изменение потенциала с расстоянием от поверхности электрода ( диффузный tyi - потенциал ( а и строение д. э. с. ( б. [4] |
Эти ионы расположены в растворе на расстоянии радиуса d сольва-тированного иона от поверхности электрода. [5]
По распространенным представлениям быстрый водородный обмен связывают с электролитической диссоциацией, в результате которой сольва-тированные ионы Н и D ( или ОН - и OD -) перераспределяются между обоими обменивающимися веществами. [6]
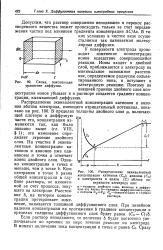 |
Распределение эквивалентной концентрации катионов ( Ск, анионов ( Са и электролита в целом ( С вблизи поверхности электрода mm. [7] |
У поверхности электрода происходит изменение концентрации ионов вследствие совершающейся реакции. Ионы входят в двойной слой, приближаются к электроду на минимальное возможное расстояние, определяемое радиусом сольва-тированного иона, и вступают в электродную реакцию. [8]
Эта схема неправильна и была потом оставлена. При сольватации ионов происходят другие процессы. Хотя в растворе действительно существуют не просто ионы Na, а сольва-тированные ионы Nac, но механизм их образования иной, чем у Пфейфера и Вернера. [9]
Различие заключается в том, что в случае реакции SN2 входящая и уходящая группы так сильно координированы с атомом углерода, что уходящая группа не может заместиться другим нуклеофи-лом, прежде чем произойдет превращение в продукты реакции. Таким образом не может образоваться симметрично построенная частица, и наблюдается обращение. Столь сильная координация означает также, что центральный атом углерода не приобретает заметного положительного заряда. В случае сольва-тированного иона карбония время жизни промежуточной частицы достаточно велико для того, чтобы другая молекула растворителя успела заменить уходящую группу. Координация в этом случае достаточно слаба, так что есть основания считать, что атом углерода несет полный положительный заряд. [10]
Первоначально в качестве комплексных соединений рассматривали неорганические комплексы с комплексообразующим ионом металла. Однако это понятие значительно шире, так что молекулярные соединения между органическими дипольными молекулами также следует считать комплексными соединениями. Педерсен [5] исследовал пикрат анилина как пример ступенчатого образования органического молекулярного соединения. В системе неорганических комплексов М представляет собой сольватированный центральный ион и МАдг - координационно насыщенный комплексный ион. Образование комплексного иона, надо полагать, происходит во всех возможных промежуточных ступенях, причем оно связано с отщеплением соответствующего числа молекул растворителя. Комплексные соединения, образованные ионами металла и ионами растворителя ( в водных растворах - это гидроксо-комплексы) представляют исключение, так как оии могут образовываться непосредственно из сольва-тированных ионов металла отщеплением иоеов водорода. [11]
Первоначально в качестве комплексных соединений рассматривали неорганические комплексы с комплексообразуюшим ионом металла. Однако это понятие значительно шире, так что молекулярные соединения между органическими дипольными молекулами также следует считать комплексными соединениями. Педерсен [5] исследовал пикрат анилина как пример ступенчатого образования органического молекулярного соединения. В системе неорганических комплексов М представляет собой сольватированный центральный ион и МАдг-координационно насыщенный комплексный ион. Образование комплексного иона, надо полагать, происходит во всех возможных промежуточных ступенях, причем оно связано с отщеплением соответствующего числа молекул растворителя. Комплексные соединения, образованные ионами металла и ионами растворителя ( в водных растворах - это гидроксо-комплексы) представляют исключение, так как они могут образовываться непосредственно из сольва-тированных ионов металла отщеплением ионов водорода. [12]
Превращение центров кристаллизации в более крупные частицы происходит, в основном, за счет диффузии вещества к поверхности и последующего осаждения. Если бы скорость диффузии в растворе была лимитирующей стадией, то скорость роста кристаллов ( за исключением тех случаев, когда имеет место высокая степень пересыщения), была бы выше, чем обычно наблюдается. Марк [33], тщательно исследовавший процесс роста кристаллов, показал, что в большинстве случаев этот процесс второго порядка, а не первого, как это соответствует диффузионному механизму. По достижении некоторой определенной скорости перемешивания, скорость роста кристаллов становится независимой от скорости перемешивания. Рост кристаллов часто задерживается или совсем подавляется вследствие адсорбции на них красителей, тогда как на скорость растворения они не оказывают заметного влияния. Это указывает, что какой-то другой фактор, а не диффузия, решающим образом определяет скорость роста кристаллов, особенно в случае мелких частиц, для которых характерно наивысшее значение диффузионного потока. Скорость потери молекул растворителя сольва-тированными ионами ряда металлов намного меньше, чем скорость диффузии [34], и высвобождение растворителя может стать фактором, контролирующим скорость роста. Если в растворе присутствуют посторонние вещества, индукционный период, скорость роста кристаллов и даже форма кристаллов могут измениться. Например, добавление желатина при осаждении сульфата бария значительно удлиняет индукционный период и снижает скорость роста кристаллов. Дейвис и Нанколлас [36] обнаружили, что многие органические вещества, например бензоат калия, даже при низких концентрациях уменьшают скорость перекристаллизации хлорида серебра. Эозин может вообще предотвратить рост кристаллов. [13]
Страницы: 1