Хемосорбированный ион
Cтраница 2
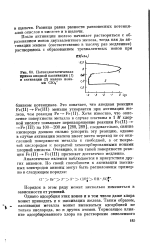 |
Потенциостатическая кривая анодной пассивации ( 1 и активации ( 2 железа ионами СЮ4. [16] |
Хотя известно, что окисление поверхности металла в случае платины в 1 М хлорной кислоте повышает перенапряжение реакции Fe ( II) - - Fe ( III) на 100 - 200 лее [288, 289], следовательно, снятие кислорода должно сильно ускорять эту реакцию, однако в случае активации железа имеет место переход не от окисленной поверхности металла к свободной, а от покрытой кислородом к покрытой хемосорбированными ионами хлорной кислоты. Очевидно, и на такой поверхности реакция Fe ( II) - - Fe ( III) протекает достаточно медленно. [17]
В литературе последних лет [10,11] всестороннему обсуждению было подвергнуто явление образования заряженного поверхностного слоя при хемосорбции. Например, в случае V2Os возникновение на поверхности хемосорбированных ионов О2 - создает вблизи поверхности электрическое поле и понижает в смежных областях концентрации квазисвободных электронов ( электронов проводимости), а также кислородных дефектов решетки Oi -, на которых в соответствии с диаграммой энергетических уровней рис. 1 локализованы электроны. Эта простая картина объясняет, по крайней мере качественно, тот экспериментально установленный факт, что в случае V Os сопротивление постоянному току определяется в первую очередь границами между зернами. В присутствии воздуха или кислорода концентрация дефектов на поверхности становится меньше, чем в объеме, а так как ток и в пленках, и в порошках должен проходить через границы между зернами, то эти границы и представляют собой основной фактор в общем сопротивлении. В присутствии этилена или ксилола концентрация дефектов на поверхности увеличивается, что сопровождается уменьшением общего сопротивления. [18]
Авторы теории образования граничного слоя при хемосорбции на полупроводниках высказали некоторые предположения в отношении того, каким должно быть в этом случае уравнение скорости процесса. Если, как полагают в этой теории, лимитирующей стадией является образование хемосорбированного иона, то задача состоит в определении скорости перемещения к краю барьера электронов или дырок из твердой фазы и последующей скорости пересечения ими барьера с переходом в адсорбированную фазу. По мере протекания адсорбции высота барьера увеличивается и перенос электрона, приводящий к дальнейшей адсорбции, становится все труднее; таким образом, в общих чертах эта теория удовлетворяет основным требованиям кинетики Рогинского - Зельдовича. [19]
Гельмгольца, прямо пропорциональна концентрации в объеме. По аналогии, скажем, с адсорбцией калия на вольфраме можно считать, что это не так и что относительные количества хемосорбированных ионов и воды должны изменяться по мере заполнения поверхности. [20]
Если в результате хемосорбции кислорода работа выхода у вольфрама сильно возрастет, то на его поверхности будут хемосорби-роваться в виде ионов не только атомы щелочных и щелочноземельных металлов, но и атомы металлов, обладающих значительно более высокими энергиями ионизации. Подобные явления имеют место также При воздействии кислорода на поверхности железа, меди и никеля, когда ионы этих металлов при своем движении по поверхности приближаются к хемосорбированным ионам кислорода или располагаются поверх них ( раздел VII, 6), вызывая проникновение хемосорбированного кислорода внутрь поверхностных слоев металла; при этом происходит обращение поверхностного потенциала. Цезий, адсорбированный поверх кислорода, хемосорбированного на вольфраме, значительно прочнее связывается с металлом, чем цезий, хемосорбированный на чистой поверхности вольфрама. [21]
Если в результате хемосорбции кислорода работа выхода у вольфрама сильно возрастет, то на его поверхности будут хемосорби-роваться в виде ионов не только атомы щелочных и щелочноземельных металлов, но и атомы металлов, обладающих значительно более высокими энергиями ионизации. Подобные явления имеют место также при воздействии кислорода на поверхности железа, меди и никеля, когда ионы этих металлов при своем движении по поверхности приближаются к хемосорбированным ионам кислорода или располагаются поверх них ( раздел VII, 6), вызывая проникновение хемосорбированного кислорода внутрь поверхностных слоев металла; при этом происходит обращение поверхностного потенциала. Цезий, адсорбированный поверх кислорода, хемосорбированного на вольфраме, значительно прочнее связывается с металлом, чем цезий, хемосорбированный на чистой поверхности вольфрама. [22]
 |
Изменение формы электрокапил-лпрной кривой ( 1 при адсорбции катионов ( 2, анионов ( 3 и нейтральных молекул ( 4. [23] |
В максимуме электрокапиллярной кривой плотность зарядов равна нулю, потенциал максимума наз. В нулевой точке отсутствует двойной электрич. В отсутствие хемосорбированных ионов разности нулевых точек различных металлов можно рассматривать как величины, аналогичные контактным разностям потенциалов, однако измеренные не в вакууме, а в лек-ром растворителе. При потенциалах, отличных от фтп отталкивание одноименных зарядов, имеющихся на поверхности, приводит к снижению величины ст. Больший наклон электрокапиллярной кривой при потенциалах, более положительных, чем рнч обусловлен большей емкостью двойного электрич. Дифференциальная емкость двойного слоя может быть измерена непосредственно или получена из электроканиллярной кривой двукратным дифференцированием. Последний способ менее точен. [24]
Кривая 1 отражает неизменяющийся во времени спектр до обработки водой. При обработке парами воды в условиях 80 % относительной влажности и 30 характерный спектр полностью исчезал, как показывают кривые 2 и 6, совпадающие с фоном. Это явление поразительно демонстрирует легкую обратимость реакции паров воды с хемосорбированными ионами карбония; оно показывает, что участвующая в реакции вода должна быть фактически очень непрочно связанной с поверхностью. [25]
Из этих рассуждений следует, что в опытах по хемосорбции или по кислородному обмену поверхностный заряженный слой является доминирующим фактором. Однако присутствие молекулы углеводорода существенно меняет эту картину. Было показано, что ксилол отдает поверхности электрон, образуя положительный хемосорбированный ион, причем как ксилол, так и этилен могут создавать в твердом теле дефекты путем потребления кислорода в реакциях их каталитического окисления. В этих условиях поверхностный заряженный слой изменяется коренным образом, и концентрация дефектов становится зависимой от природы адсорбированного углеводорода и от степени протекания реакции, которая происходит скорее, чем в случае зависимости только от концентрации кислорода. [26]
Таким образом, изменения уровня Ферми при легировании компенсируются на поверхности равными, но противоположными изменениями электрического потенциала. Эти результаты уже объясняют некоторые особенности измерений уровня Ферми на поверхности, проведенных Клиером, а также Белянским и Деренем. Исходя из нашего второго приближения, при котором рассматриваются сферические эквипотенциальные уровни вокруг хемосорбированных ионов кислорода, можно убедиться в слабой миграции дырок из объема на поверхность. Поскольку в данном случае поверхностная концентрация дырок изменяется от одной стороны поверхности к другой, уровень Ферми на поверхности нельзя считать одним и тем же, а следует рассматривать только среднее значение уровня Ферми на поверхности. [27]
Гудри имеются как бренстедовские, так и льюисовские центры. Эти результаты были подтверждены Базила и др. [363], применившими тот же метод. Обработка ацетатом калия ослабляет кислотность большинства льюисовских центров и полностью уничтожает бренстедовские центры. Вода, необратимо адсорбировавшаяся при комнатной температуре, превращала координационно связанный пиридин в ионы пиридиния. Аналогичный эффект наблюдали Лефтин и Холл [364]: электронный спектр хемосорбированных ионов карбония исчезал при добавлении воды и вновь появлялся после непродолжительной откачки. Модель, сформулированная Базила и др. [363], предполагает, что все первичные кислотные центры являются льюисовскими, локализованными на ионе алюминия, а предполагаемые бренстедовские центры образуются при вторичном взаимодействии между молекулами, адсорбированными на льюисовских центрах, и соседними поверхностными гидроксиль-ными группами, являющимися силанольными. [28]
Рассматривается влияние электронного фактора в реакциях высокотемпературного окисления СО и Н2 на катализаторах из закиси никеля, непромотированной и промотированной окисью лития или окисью галлия. Обсуждение результатов проведено на основании улучшенной теории, базирующейся на новы. Сравнение скоростей реакций с концентрацией дырок в катализаторе обнаруживает сходное изменение этих параметров. Кроме того, количество хемосорбированного кислорода не зависит от концентрации дырок. Для теоретического анализа используются кинетические уравнения, в которые входит концентрация дырок на поверхности катализатора. Что касается искривления потенциального уровня у поверхности; то эта величина связана с концентрацией дырок в объеме катализатора. Обнаружена тесная связь между хемосорбированными ионами кислорода л дырками в граничном слое. Сделан вывод, что ионы N1, расположенные рядом с местами хемосорбции кислорода, являются центрами реакции. Стадией, определяющей скорость процесса, является захват дырок в результате удара из объема или физической адсорбции молекул СО или Hj. Все экспериментальные данные автора находятся в удовлетворительном согласии с этой теорией. [29]
Страницы: 1 2