Гейдельбергер
Cтраница 1
Гейдельбергер и др. [229, 230] показали, что F3T может количественно гидролизоваться в растворе бикарбоната с образованием 5-карбоксиурацила, но что F3TdR гидролизуется до 5-карбоксиурацила с весьма небольшим выходом. На рис. 6.10 показано, как происходит гидролиз. [1]
Гейдельбергера и его школы недостаточно чувствителен. [2]
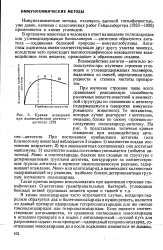 |
Кривая осаждения. [3] |
Иммунохимические методы, отличаясь высокой специфичностью, уже давно, начиная с классических работ Гейдельбергера ( 1923 - 1929) применяются в химии углеводов. [4]
Так как свойства этого углеводорода могли пролить некоторый свет на строение бензола, Вильштеттер и Вазер ( 1911) и Гейдельбергер - ( 1913) осуществили синтез циклооктатетраена из псевдопельтьерина. [5]
Так как свойства этого углеводорода могли пролить некоторый свет на строение бензола, Вильштетгер и Вазер ( 1911) и Гейдельбергер ( 1913) осуществили синтез циклооктатетраена из псевдопельтьерина. [6]
Так, Волфром ( 1947, 1952) выделил из легких крупного рогатого скота после удаления гепарина галактан и показал, что последний состоит в основном из D-галактозы. Гейдельбергер нашел ( 1955), что галактан, выделенный из легких, как и предполагалось, образует осадок с полисахаридом пневмококков типа XIV. Однако галактан давал также положительную реакцию преципитации и с полисахаридом пневмококков типа II, состоящим из L-рамнозы, D-глюкозы и D-глюкуроновой кислоты. [7]
О том, что кинуренин является нормальным метаболитом триптофана, свидетельствует также тот факт, что это соединение представляет собой промежуточный продукт при превращении триптофана в никотиновую кислоту. Бидл, Мит-чел и Найе [300], а также Гейдельбергер, Абрагам и Лепковский [301] доказали, что кинуренин является промежуточным соединением при превращении триптофана в никотиновую кислоту. Следовательно, доказано, что кинурепин является необходимым промежуточным продуктом при метаболизме триптофана. [8]
Высокая типовая специфичность является характерной чертой многих подобных полисахаридов. Значение этого обстоятельства для медицины не требует разъяснений; этим свойством чрезвычайно остроумно пользуется также Гейдельбергер [37] при изучении одной из наиболее актуальных и трудных проблем химии полисахаридов. Если тщательно очищенное вещество дает при гидролизе несколько различных Сахаров, часто еще бывает трудно определить, является ли это вещество одним полисахаридом или же смесью сахаридов сходного типа. Если имеются группы, реагирующие со специфической антисывороткой, осадок будет содержать все остатки, входящие в состав реагента-полисахарида. Если исходное вещество является смесью, очень может быть, что только один из полисахаридов выпадает в осадок, и количественный анализ остатков сахара в осадке, по сравнению с анализом исходного вещества, покажет отсутствие гомогенности. Этот метод уже оправдал себя; он и в будущем может иметь большое значение. Кроме того, развитие этого метода помогает проиллюстрировать одну особую черту химии углеводов на ее современном уровне: подробные сведения о свойствах Сахаров, полученные в результате работ химиков-органиков, теперь используются в медицине, биохимии и биологии для разгадки той чрезвычайно сложной роли, которую играют углеводы в превращении живой материи. Заглядывая в будущее, мы ясно видим, что дальнейшие успехи в области изучения этой обширной, но еще пока не освоенной области возможны только при тесном сотрудничестве химиков, физиков и биологов. [9]
Так как способность к перекрестной реакции зависит от структурного сходства полисахаридов, то иммунологическая реакция успешно применяется при структурных исследованиях. Так, Волфром ( 1947, 1952) выделил из легких крупного рогатого скота после удаления гепарина галактан и показал, что последний состоит в основном из D-галактозы. Гейдельбергер нашел ( 1955), что галактан, выделенный из легких, как и предполагалось, образует осадок с полисахаридом пневмококков типа XIV. Однако галактан давал также положительную реакцию преципитации и с полисахаридом пневмококков типа II, состоящим из L-рамнозы, D-глюкозы и D-глюкуроновой кислоты. В дальнейшем при помощи бумажной хроматографии было показано, что галактан, выделенный Волфромом из легких крупного рогатого скота, неоднороден и загрязнен примесями, содержащими D-глюкуро-новую кислоту. [10]
Остается рассмотреть реакции сочетания аминохи ноли нов с диазосоедине-ниями. Кнюппель [563] сочетал 6-аминохинолин с Хлористым фенилдиазони-ем, получив при этом диазоаминосоединение, не способное к перегруппировке. Согласно Якобсу и Гейдельбергеру [ 531а ], сочетание 5-аминохинолина и 6-метокси - 5-аминохинолина с диазосоединениями в разбавленной уксусной кислоте и растворе ацетата натрия приводит к получению 8-азосоединений. Реншау, Фридман и Гаевский [564] провели исчерпывающее исследование этой реакции для всех аминохинолинов. [11]
В природных фосфо-протеидах фосфор связан прочно, но полностью отщепляется при длительной обработке щелочью. В казеине и вителлине фосфор связан с алифатическими гидроксильными группами, и в этом случае можно выделить фосфосерин. Хотя гидроксильные группы могут также реагировать с РОСЦ, Майер и Гейдельбергер показали, что по крайней мере половина фосфатных остатков в фос-форилированном сывороточном альбумине либо связана с аминогруппами, либо маскирует их, защищая от воздействия азотистой кислоты. Качественным доказательством этерификации остатков тирозина служило уменьшение интенсивности окраски при реакции Фолина. [12]
В разработанном Римингтоном [133] методе фосфорилирования к раствору белка при 0 по каплям добавляют хлорокись фосфора ( РОС13), растворенную в четыреххлористом углероде, и поддерживают рН раствора в пределах 8 5 - 9 путем постепенного прикапывания концентрированного раствора NaOH. В отличие от природных фосфопротеидов в синтетических фосфопротеидах большая часть фосфора удерживается лабильными связями. Этим методом был получен фосфорилированный яичный альбумин [134] и изучена кривая его титрования. Так как этот белок был, по-видимому, денатурирован, то Майер и Гейдельбергер [47] изучили условия фосфорилирования сывороточного альбумина, надеясь таким образом избежать осложняющего влияния денатурации. [13]
Полное дезаминирование не было достигнуто ни в одном случае. Физическое и химическое исследования этих двух фракций дезаминированного белка показали, что фракция Б, у которой удалена только одна треть аминогрупп, по своему оптическому вращению, вязкости, молекулярному весу и отношению постоянных трения сходна с нативным белком и, следовательно, может быть названа неденатурированным дезаминированным белком. Маурер и Гейдельбергер считают, что денатурация обусловлена дезаминированием существенно важных для структуры белка аминогрупп, которые начинают реагировать только после того, как прореагировали более легко доступные функциональные группы. Однако, как указывалось выше и было признано Мауре-ром и Гейдельбергером [1246], реакция азотистой кислоты с белками весьма неспецифична. Дезаминированные фракции всегда имели желтый цвет благодаря введению хромофорных нитрозо -, азо - или диазогрупп в остатки ароматических аминокислот. Таким образом, заключение о роли аминогрупп в сохранении нативной структуры яичного альбумина являются сомнительным. [14]
Полное дезаминирование не было достигнуто ни в одном случае. Физическое и химическое исследования этих двух фракций дезаминированного белка показали, что фракция Б, у которой удалена только одна треть аминогрупп, по своему оптическому вращению, вязкости, молекулярному весу и отношению постоянных трения сходна с нативным белком и, следовательно, может быть названа неденатурированным дезаминированным белком. Маурер и Гейдельбергер считают, что денатурация обусловлена дезаминированием существенно важных для структуры белка аминогрупп, которые начинают реагировать только после того, как прореагировали более легко доступные функциональные группы. Однако, как указывалось выше и было признано Мауре-ром и Гейдельбергером [1246], реакция азотистой кислоты с белками весьма неспецифична. Дезаминированные фракции всегда имели желтый цвет благодаря введению хромофорных нитрозо -, азо - или диазогрупп в остатки ароматических аминокислот. Таким образом, заключение о роли аминогрупп в сохранении нативной структуры яичного альбумина являются сомнительным. [15]
Страницы: 1