Гейтлер
Cтраница 2
Гейтлер и Лондон предположили, что достаточно хорошим приближением к истинному виду волновой функции в молекуле водорода будет выражение, учитывающее возможность движений электронов, выражаемых обоими соотношениями. [16]
Гейтлер и Лондон проводили расчет так называемым методом возмущений; однако к тем же результатам приводит вариационный метод, о которой было сказано выше. Этот метод является более простым, и в последующих более точных квантовомеханических расчетах молекулы водорода другие исследователи использовали вариационный метод. [17]
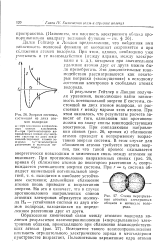 |
Энергия системы, состоящей из двух атомов водорода. [18] |
Далее Гейтлер и Лондон предположили, что найденная ими зависимость волновой функции от координат сохраняется и при сближении атомов водорода. При этом, однако, необходимо уже учитывать и те взаимодействия ( между ядрам. [19]
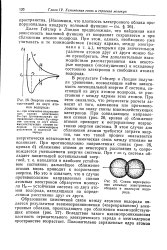 |
Энергия системы, состоящей из двух атомов водорода. [20] |
Далее Гейтлер и Лондон предположили, что найденная ими зависимость волновой функции от координат сохраняется и при сближении атомов водорода. [21]
Расчет Гейтлера и Лондона дал количественное объяснение химической связи на основе квантовой механики. Он показал, что если электроны атомов водорода обладают противоположно направленными спинами, то при сближении атомов происходит значительное уменьшение энергии системы - возникает химическая связь. Образование химической связи обусловлено тем, что при наличии у электронов антипараллельных спинов становится возможным передвижение электронов около обоих ядер, которое иногда не вполне удачно называют обменом электронов. Движение электронов около обоих ядер приводит к значительному увеличению плотности электронного облака в пространстве между ядрами, которое стягивает положительно заряженные ядра. Следовательно, образование химической связи объясняется понижением потенциальной энергии электронов, обусловленным увеличением плотности электронного облака в пространстве между ядрами. [22]
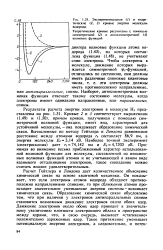 |
Экспериментальная ( / и теоретические ( 2, 3 кривые энергии молекулы водорода. [23] |
Расчет Гейтлера и Лондона дает количественное объяснение химической связи на основе квантовой механики. Он показывает, что если электроны атомов водорода обладают противоположно направленными спинами, то при сближении атомов происходит значительное уменьшение энергии системы - возникает химическая связь. Образование химической связи обусловлено тем, что при наличии у электронов антипараллельных спинов становится возможным движение электронов около обоих ядер. Движение электронов около обоих ядер приводит к значительному увеличению плотности электронного облака в пространстве между ядрами, что, в свою очередь, вызывает стягивание положительно заряженных ядер. [24]
Представления Гейтлера и Лондона о механизме образования химической связи оказались чрезвычайно плодотворными и послужили основой для объяснения и приближенного расчета связи в более сложных молекулах. [25]
 |
Экспериментальная ( / и теоретические ( 2, 3 кривые энергии молекулы водорода. [26] |
Расчет Гейтлера и Лондона дает количественное объяснение химической связи на основе квантовой механики. Он показывает, что если электроны атомов водорода обладают противоположно направленными спинами, то при сближении атомов происходит значительное уменьшение энергии системы - возникает химическая связь. Образование химической связи обусловлено тем, что при наличии у электронов антипараллельных спинов становится возможным движение электронов около обоих ядер. Движение электронов около обоих ядер приводит к значительному увеличению плотности электронного облака в пространстве между ядрами, что, в свою очередь, вызывает стягивание положительно заряженных ядер. [27]
Представления Гейтлера и Лондона о механизме образования химической связи оказались чрезвычайно плодотворными и послужили основой для объяснения и приближенного расчета связи в более сложных молекулах. [28]
Расчеты Гейтлера - Лондона ( Heitler - London) показали, что мерой гомеополяр-ной валентности атома во многих случаях служит число так называемых неспаренных электронов. [29]
Расчеты Гейтлера - Лондона ( Heitler - London) показали, что мерой гомеополяр-ной валентности атома во многих случаях служит число так называемых неспаренных электронов. Например, у Не в нормальном состоянии оба электрона спарены ( ср. Литий, наоборот, как и Н, обладает неспаренным электроном; поэтому литий может ( кроме гетерополярных) образовать также гомеополярные соединения. [30]
Страницы: 1 2 3 4