Одновалентный ион - медь
Cтраница 3
Однако отсюда не следует, что акцепторами служат входящие в закись меди атомы кислорода. Вероятно, избыточно поглощенный кислород переводит часть одновалентных ионов меди в двухвалентные ионы, на которые тепловое движение переносит затем электроны из заполненной полосы. Возможно также, что диффундирующие к поверхности ионы меди соединяются там с кислородом, оставляя свободные узлы в решетке закиси. [31]
Основным требованием к анодам в таких электролитах является их растворение без шлама. Причинами шламо-образования могут быть накопление в растворе одновалентных ионов меди, вызывающих выпадение мелких частиц или вытравливание с поверхности анодов кристаллов меди. [32]
Строгое описание анодного процесса требует рассмотрения реакций ( 57 - 2) и ( 57 - 3) как одновременных ( разд. При этом анализ усложняется необходимостью учета диффузии и конвекции одновалентных ионов меди, для чего следует рассматривать процессы переноса, описанные в части В. [33]
Повышение температуры электролита позволяет работать при более высоких плотностях тока. Обычно при этом повышают также и кислотность электролитов, так как повышение температуры благоприятствует образованию одновалентных ионов меди. [34]
Поскольку реакция ( 57 - 2) быстрее реакции ( 57 - 3), восстановление одновалентного иона меди будет протекать одновременно с восстановлением двухвалентных ионов меди до одновалентных и можно будет различить лишь одну полярографическую волну. С другой стороны, реакция ( 59 - 2) быстрее реакции ( 59 - 3), и при восстановлении кислорода наблюдаются обе волны. [35]
Во время опыта плотность тока необходимо поддерживать в заданных пределах. Если она будет меньше 0 01 А / см2, то выделится слишком мало металла, так как будут частично образовываться одновалентные ионы меди. При слишком высокой плотности тока сцепление покрытия с электродом будет слабым и при извлечении электрода из раствора оно может осыпаться. [36]
Во время опыта плотность тока необходимо поддерживать в заданных пределах. Если она будет меньше 0 01 А / см2, то выделится слишком мало металла, так как будут частично образовываться одновалентные ионы меди. При слишком высокой плотности тока сцепление покрытия с электродом будет слабым и при извлечении электрода из раствора оно может осыпаться. [37]
Чем ниже температура электролита, выше анодная плотность тока и меньше концентрация свободного цианида ( в отсутствие сегнетовой соли и роданида), тем скорее пассивируются аноды, покрываясь пленкой CuCN. При этом анодный потенциал сильно смещается в сторону положительных значений, выход меди по току и концентрация ее в растворе снижаются. Наряду с этим происходит окисление одновалентных ионов меди до двухвалентных и цианида в циа-наты, что вызывает излишний расход цианида натрия или калия. [38]
Чем ниже температура электролита, выше анодная плотность-тока и меньше концентрация свободного цианида ( в отсутствие сегнетовой соли и роданида), тем скорее и полнее пассивируются аноды, покрываясь пленкой CuCN или дицианидов. При этом анодный потенциал сильно смещается в сторону положительных значений, выход меди по току падает и концентрация ее в растворе снижается. Наряду с этим происходит окисление одновалентных ионов меди до двухвалентных и цианида в цианаты, что приводит к лишнему расходу цианистого натрия или калия. [39]
Чем ниже температура электролита, выше анодная плотность тока и меньше концентрация свободного цианида ( в отсутствие сегнетовой соли и роданида), тем скорее пассивируются аноды, покрываясь пленкой CuCN. При этом анодный потенциал сильно смещается в сторону положительных значений, выход меди по току и концентрация ее в растворе снижаются. Наряду с этим происходит окисление одновалентных ионов меди до двухвалентных и цианида в циа-наты, что вызывает излишний расход цианида натрия или калия. [40]
Чем ниже температура электролита, выше анодная плотность тока и меньше концентрация свободного цианида ( в отсутствие сегнетовой соли и роданида), тем скорее пассивируются аноды, покрываясь пленкой CuCN или парациа-нида. При этом анодный потенциал сильно смещается в сторону положительных значений, выход меди по току падает и концентрация ее в растворе снижается. Наряду с этим происходит окисление одновалентных ионов меди до двухвалентных и цианида в цианаты, что вызывает излишний расход цианистого натрия или калия. [41]
 |
Зависимость lg kz f ( 1 / Г для окисления меди в кислороде. [42] |
Валенси, энергии активации, вычисленные для высокотемпературного и низкотем -, пературного участков графика, равны соответственно 37 7 и 20 1 ккал / г-атом. В условиях высокотемпературного окисления окись меди неустойчива, так что закись меди Си2О остается единственным присутствующим окислом. Найденное Кастелланом и Моором значение теплоты активации для диффузии одновалентных ионов меди в Си2О, равное 37 8 ккал / г-атом, является убедительным доказательством того, что этот диффузионный процесс определяет скорость высокотемпературного окисления меди. [43]
Валенси [261], энергии активации, вычисленные для высокотемпературного и низкотемпературного участков графика, оказались равны соответственно 37700 и 20140 кал. В условиях высокотемпературного окисления окись меди неустойчива, так что закись меди CU2O остается единственным присутствующим окислом. Найденное Кастелланом и Моором [262] значение теплоты активации для диффузии одновалентных ионов меди в Си2О, равное 37800 кал, является убедительным доказательством того, что этот диффузионный процесс определяет скорость высокотемпературного окисления меди. [44]
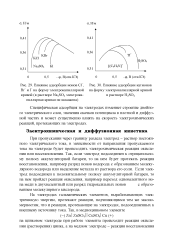 |
Влияние адсорбции ионов С1, [ IMAGE ] Влияние адсорбции катионов. [45] |
Страницы: 1 2 3 4