Гексанола
Cтраница 2
Исирикян, Киселев и Ушакова [306] опубликовали данные по хемосорбции метанола или гексанола на термически обработанной поверхности ТЮ2 с образованием поверхностных эфиров. [16]
Навеску фторсодержащего соединения ( 10 - 20 мг) растворяют в 15 мл гексанола в колбе, снабженной обратным холодильником, и после прибавления 0 2 г металлического натрия нагревают смесь 15 мин до кипения. [17]
Для этого после измерения объема образовавшегося метана в реакционную смесь вводят в избытке гексанол, анилин gi или воду 12 и определяют дополнительное количество выделившегося метана. [18]
Основное отличие предлагаемого способа от существующих - применение сравнительно неглубоких вакуума и присадки - гексанола. [19]
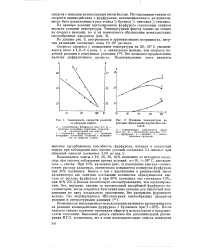 |
Зависимость скорости реакции от природы спирта.| Влияние температуры на. [20] |
Исследованные спирты по скорости взаимодействия с фурфуролом, катализированного катионитом, могут быть расположены в ряд: этанол бутанол пентанол гексанол. [21]
Так, при нагревании стехиометрнческих количеств карбамида и ароматического амина до 100 - 200 С в высококипящем спирте, например, феноле, гексаноле, циклогексаноле [57] образуется соответствующее арилпроизводное. Недостатком этого метода является взаимодействие растворителя с изоцианатом - промежуточным продуктом реакции, что приводит к увеличению расхода растворителя и загрязнению конечного продукта уретаном. Во избежание этого предлагается [58 ] осуществлять синтез в среде 1, 2, 4-трихлорбензола. По этому способу карбамид в указанном растворителе обрабатывают двукратным ( по отношению к стехио-метрическому) количеством парахлоранилина, после чего полученную реакционную массу обрабатывают избыточным количеством диметиламина. В результате получается монурон без примеси уретана. [22]
 |
Давление пара изотопных вторичных бутанолов Р, тм рт. ст. [23] |
Ясно, что эти данные не соответствуют друг другу, так как согласно им разность теплот парообразования этанола и метанола составляет около 1140 кал / моль, гексанола и пентанола 1420, октанола и гексанола 2410, а теплоты парообразования про-панола и этанола различаются только на 480, бутанола и пропанола - лишь на 260 кал / моль. По-видимому, данные [223] для пропанола и бутанола неверны. Это подтверждается приведенной в работе [225] величиной теплоты парообразования пропанола для 0 С 11 630 кал / моль. Можно также отметить, что в результате обработки данных ряда работ для теплоты парообразования того же спирта при 80 С получена величина 10 400 кал / моль [225], а по уравнению (1.68) для 80 С получается 10 460 кал / моль. [24]
Кудрейко и др. [331] исследовали влияние спиртов на поведение ненасыщенных дикарбоновых кислот методом хронопотенцио-метрического титрования; оценены значения показателей констант ионизации дикарбоновых кислот и определены значения pKs бу-танола, пентанола, гексанола и октанола. [25]
 |
Давление пара изотопных вторичных бутанолов Р, тм рт. ст. [26] |
Ясно, что эти данные не соответствуют друг другу, так как согласно им разность теплот парообразования этанола и метанола составляет около 1140 кал / моль, гексанола и пентанола 1420, октанола и гексанола 2410, а теплоты парообразования про-панола и этанола различаются только на 480, бутанола и пропанола - лишь на 260 кал / моль. По-видимому, данные [223] для пропанола и бутанола неверны. Это подтверждается приведенной в работе [225] величиной теплоты парообразования пропанола для 0 С 11 630 кал / моль. Можно также отметить, что в результате обработки данных ряда работ для теплоты парообразования того же спирта при 80 С получена величина 10 400 кал / моль [225], а по уравнению (1.68) для 80 С получается 10 460 кал / моль. [27]
Какие карбонильные соединения получатся в результате окисления или каталитического дегидрирования: а) 1-бутанола; б) 2-бутанола; в) 2-метил - 1-бута нола; г) 2 4-диметил - 1-пентанола; д) З - метил-1 - гексанола; е) 2-метил - 3-пентанола; ж) 4 4-диметил - З - гексанола; з) триме-тиленгликоля; и) 2 4-пентандиола; к) 2 5-гептандиола. [28]
Депарафинизацию проводили следующим образом: неочищенный дистиллят разбавляли метиленхлоридом ( от 50 - 100 %), затем в него подавали кристаллический карбамид 100 % предварительно смоченный водой ( 10 - 12 %) или метанолом ( 2 - 3 %) с добавкой 0 1 % гексанола. [29]
Какие карбонильные соединения получатся в результате окисления или каталитического дегидрирования: а) 1-бутанола; б) 2-бутанола; в) 2-метил - 1-бута нола; г) 2 4-диметил - 1-пентанола; д) 3-метил - 1-гексанола; е) 2-метил - 3-пентанола; ж) 4 4-диметил - З - гексанола; з) триме-тиленгликоля; и) 2 4-пентандиола; к) 2 5-гептандиола. [30]
Страницы: 1 2 3 4