Гексафторантимонат
Cтраница 1
Гексафторантимонат, гексафторарсенат и тетра-фторборат перфтораммония представляют собой белые кристаллические вещества. По данным рентгенографического анализа, гексафторарсенат тетрафтораммония имеет кристаллическую структуру, сходную со структурой PCl / PClg, элементарная ячейка имеет параметры: а 7 70 А, с - 5 73 А. Кристаллы тетрафторбората относятся к кубической сингонии, параметр а 7 53 А. [1]
Гексафторантимонат перфтораммония получается из этих солей нагреванием их в вакууме при 200 С в течение 3 дней. [2]
Образование гексафторантимоната серебра подтверждено [72] кондуктометрическим титрованием бромтетрафторида серебра сурьмяной кислотой в трифториде брома. [3]
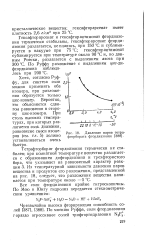 |
Давление паров тетра-фторбората фтордиазония. [4] |
Гексафторарсенат и гексафторантимонат фтордиазония термически стабильны, гексафторарсенат фтордиазония разлагается, не плавясь, при 150 С и сублимируется в вакууме при 75 С; гексафторантимонат сублимируется при температуре около 90 С и, по данным Роески, разлагается с выделением азота при 300 С. [5]
Предварительные исследования химических свойств гексафторантимоната перфтораммония выполнили Панкратов и Аханщикова. [6]
Транс-изомер дифтордиазина получается также при разложении гексафторантимоната трифторгидразония N2F3SbFe, который синтезируется из тетрафторгидр-азина и пятифтористой сурьмы ( см. гл. [7]
Возможность получения устойчивых солей алкилкарбониевых ионов с гексафторантимонатом при взаимодействии фтористых алкилов с пятифто-ристой сурьмой ( в чистом виде или в растворах двуокиси серы, а позднее - в сульфурилфториде или сульфурилхлоридфториде) была подробно выяснена при исследовании всех изомерных фтористых С3 -, С4 - и С5 - алкилов. [8]
Имеются данные по конкурентным реакциям [41] 1-хлорфор-милапокамфана с гексафторантимонатом серебра ( I) в смесях ароматических растворителей, таких как хлорбензол - бензол, хлорбензол - толуол, бензол - толуол и хлорбензол - нитробензол. Анализ всех данных приводит к предположению, что реакция проходит через образование а-комплекса на лимитирующей стадии, даже в случае исключительно реакционноспособного электрофила. [9]
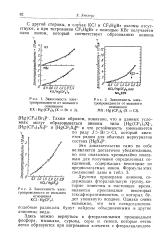 |
Зависимость электропроводности от мольного. [10] |
Другими примерами анионов, содержащих фторалкильную группу, которые известны в настоящее время, являются производные некоторых гексафторантимонатов, о которых будет упомянуто позднее. [11]
Как ИК -, так и ЯМР-характеристики для этих ионов были получены путем изучения их тетрахлоралюминатов или гексафторантимонатов. [12]
Как ИК -, так и ЯМР-характеристики для этих ионов были получены путем изучения их тетрахлоралюминатов или гексафторантимонатов. [13]
Гексафторарсенат и гексафторантимонат фтордиазония термически стабильны, гексафторарсенат фтордиазония разлагается, не плавясь, при 150 С и сублимируется в вакууме при 75 С; гексафторантимонат сублимируется при температуре около 90 С и, по данным Роески, разлагается с выделением азота при 300 С. [14]
По-видимому, особенно агрессивен тетрафторборат фтордиазония. Гексафторантимонат энергично реагирует с нитрометаном, нитробензолом, четыреххлори-стым углеродом, фреонами, двуокисью серы ( образуются SOF2, SOaF2, SOa - SbF5, N2O, N2), в жидком фтористом водороде нерастворим или растворим весьма плохо. Растворитель для него подобрать не удалось, поскольку со всеми веществами он реагирует. [15]
Страницы: 1 2