Гексафторид - ксенон
Cтраница 2
Среди гексафторидов исключение составляет гексафторид ксенона. [16]
Имеются сообщения о синтезе высшего фторида ксенона - ок-сафторида XeF8, который был выделен в качестве побочного продукта при синтезе гексафторида ксенона. [17]
Дайте правдоподобное объяснение каждого из следующих фактов: а) белый фосфор, в отличие от красного, обладает довольно большой летучестью; б) добавление SF4 к воде приводит к образованию кислого раствора; в) гексафторид ксенона является устойчивым соединением, тогда как гексафторид криптона неизвестен; г) азот широко распространен в природе в виде свободного элемента, тогда как фосфор встречается только в соединениях. [18]
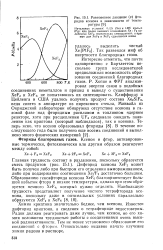 |
Равновесное давление ( р фторидов ксенона в зависимости от температуры. [19] |
Дифторид ксенона XeF2 может быть получен либо при быстром его отделении вымораживанием, либо при поддержании соотношения Xe / F2 достаточно большим. Образованию гексафторида ксенона XeF6 благоприятствует большой избыток фтора и низкие температуры, однако при этом образуется немного XeF4, который нужно отделять. [20]
 |
Структура молекул фторидов и оксидов ксенона. [21] |
Они относительно легко летучи, более всего - гексафторид ксенона. Кстати, последний является термически менее устойчивым соединением и химически весьма активным. Все фториды являются хорошими фторирующими веществами. Тетрафторид криптона - бесцветное твердое вещество, менее устойчивое, чем тетрафторид ксенона. [22]
 |
Структура молекул фторидов и оксидов ксенона. [23] |
Летучесть этих соединений свидетельствует о - ковалентном характере связей и отсутствии дипольного момента. Молекула XeF2 имеет линейное строение; оставшиеся у атома ксенона 3 пары электронов располагаются по углам равностороннего треугольника, находящегося в экваториальной плоскости к линиям связи Хе - F. Что касается гексафторида ксенона, то он представляется в виде искаженного октаэдра, на одной иа плоскостей которого имеется пара электронов. [24]
Правда, средняя величина энергии связи в молекуле гексафторида, как и в других фторидах ксенона, невелика. Во-первых, в молекуле XeF6 имеется шесть связей, а в молекуле Н2О - только две. Значит, в случае гексафторида ксенона на одну связь приходится меньшая доля общей энергии взаимодействия. Для этого требуется гораздо меньше энергии, чем для разрыва молекул О2 и Н2 - всего - 38 ккал / моль. [25]
Гидролиз тетрафторида ксенона более сложен. Преобладающей реакцией в кислой и нейтральной средах является диспропорционирова-ние Xe ( IV) до газообразного ксенона и соединения Xe ( VI) в растворе. Аналогичные соединения Xe ( VI) образуются при гидролизе гексафторида ксенона в растворе. Надежно идентифицирован ряд солей этой кислоты. С другой стороны, ксенаты и перксенаты являются очень сильными и потенциально весьма полезными окислителями. Ни одно из упомянутых соединений ксенона не окрашено, но часто при гидролизе кристаллов всех фторидов ксенона наблюдается промежуточное появление желтой окраски. Химия водных растворов фторидов ксенона, по-видимому, весьма похожа на химию соответствующих фторидов ксенона. [26]
Их могут образовывать как металлы, так и неметаллы. Двадцать известных гексафторидов-это гексафто-риды неметаллов, гексафториды металлов и стоящий особняком гексафторид ксенона. [27]
Из большого числа подобных соединений обратим внимание лишь на некоторые из них. Так, первое стабильное ионное соединение ксенона было получено в конце 1962 г. Это - гексафторид ксенона XeFe. [28]
Страницы: 1 2