Гексафторид - селен
Cтраница 1
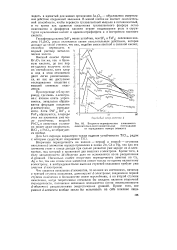 |
Вторично-периодическая зависимость. [1] |
Гексафторид селена SeF6 менее устойчив, чем SFe и TeF6; селеновая кислота HaSeO4 резко отличается своим окислительным действием, которое доходит до такой степени, что она, подобно смеси азотной и соляной кислот, способна переводить в водный раствор металлическое золото. [2]
Гексафторид селена значительно более реакционноспособен, чем гексафторид серы. [3]
Гексафторид селена способен гидролизоваться при не очень высоких температурах. [4]
Гексафторид селена SeF5, представляющий собой бесцветный газ, образуется при-76 в результате взаимодействия фтора и селена. [5]
 |
Кристаллическая структура 5еО. / опо Ч / У. [6] |
С, гексафторид селена SeF6 - молекула - окт. [7]
Положение с гексафторидами селена SeFe и теллура TeFe должно быть таким же, как и в случае гексафторида серы SFe; разница состоит в том, что связи у них должны иметь более ярко выраженный ионный характер и доля структур с двойными связями с участием 4р - и 5б / - электронов должна быть исчезающе мала. Следовательно, присоединение доноров электронов к центральному атому облегчается не только в стерическом смысле, но и в чисто электронном. Именно этим объясняется большая легкость, с которой эти соединения реагируют с основаниями. Эти же соображения могут быть использованы при рассмотрении ряда других гексафторидов и комплексных ионов типа MF6, особенно фторидов лантанидов и актинидов ( элементы 57 - 71 и 89 - 96), а также элементов подгрупп III, IV, V и VI групп в состоянии максимальной валентности. В случае гексафторидов подгрупп других групп также имеет место образование гибридных связей и у них можно ожидать отклонение симметрии от правильного октаэдра. [8]
Гексафторид теллура еще более активен, чем гексафторид селена. [9]
Из анализа работ, опубликованных до 1966 г., для теплоты образования гексафторидов селена и теллура авторами справочника [19] рекомендованы значения ДЯ / 298 ( SeFe, газ) - 246 ккал / молъ и ДЯ / 298 ( TeF6, газ) - 315 ккал / молъ соответственно. Позднее появилась работа [48], содержащая данные, заметно отличающиеся от приведенных выше значений: Д 298 ( SeFe, газ) - 226 95 0 14; ДЯ298 ( TeF6, газ) - 327 2 0 56 ккал / молъ. Работа [48] выполнена с использованием чистых исходных веществ и проведением тщательного анализа продуктов реакции, что позволяет считать полученные в ней результаты более надежными. [10]
Хлорид селена ( SeiCh) - темная красно-коричневая стабильная жидкость, во влажной среде происходит ее гидролиз с образованием селена, селенистой кислоты и соляной кислоты. Гексафторид селена ( SeFe) применяется в качестве газообразного электроизолятора. [11]
Повышение химической активности гексафторидов по мере повышения атомного веса центрального атома, невидимому, связано со структурой этих соединений. Таким образом, в гексафториде серы атом фтора образует химически устойчивую оболочку, которая предохраняет атом серы от действия веществ, являющихся донорами электронов. В гексафториде селена межатомные расстояния больше и связи более полярны, благодаря чему для достижения электронами донора атома селена требуется меньшее количество тепловой энергии. Предохраняющая оболочка вокруг атома теллура разрушается под влиянием тепловой энергии еще легче. [12]
Гексафториды возгоняются не плавясь. При обычных температурах они не действуют на стекло. Шестифтори-стый селен и теллур разъедают стекло при температуре размягчения стекла или близкой к ней. Шестифтористый теллур разлагает воду. Шестифтористая сера не действует на ртуть, в отличие от гексафторидов селена и теллура. Все гексафториды в газообразном состоянии пропускают ультрафиолетовые лучи, вплоть до самых коротких волн, даваемых кварцевым спектрографом. [13]
Гексафториды возгоняются не плавясь. При обычных температурах они не действуют на стекло. Шестифтористый селен и теллур разъедают стекло при температуре размягчения стекла или близкой к ней. Шестифтористый теллур разлагает воду. Шестифтористая сера не действует на ртуть, в отличие от гексафторидов селена и теллура. Все гексафториды в газообразном состоянии пропускают ультрафиолетовые лучи, вплоть до самых коротких волн, даваемых кварцевым спектрографом. [14]
Страницы: 1