Последний ион
Cтраница 2
Предложенные Штоком названия четырех последних ионов не получили широкого распространения, и предпочитают называть их нитрат, нитрит, сульфат и сульфит, как это было до изменения номенклатуры в 1970 г. Кислоты. [16]
В каждом случае таковым является последний ион для данного соединения в таблицах. Для бесконечно разбавленных растворов АФ перестает зависеть от этого выбора и зависит лишь от отношений концентраций ионов в краевых растворах. Растворы с нулевой ионной силой ( / г1) отмечены звездочкой, однако концентрациям приданы ненулевые значения, чтобы можно было найти эти отношения. Эти соединения составляют также основу для сравнения с более концентрированными растворами, что позволит выявить влияние коэффициентов активности. [17]
В каждом случае таковым является последний ион для данного соединения в таблицах. Для бесконечно разбавленных растворов АФ перестает зависеть от этого выбора и зависит лишь от отношений концентраций ионов в краевых растворах. Растворы с нулевой ионной силой ( fi-l) отмечены звездочкой, однако концентрациям приданы ненулевые значения, чтобы можно было найти эти отношения. Эти соединения составляют также основу для сравнения с более концентрированными растворами, что позволит выявить влияние коэффициентов активности. [18]
Было показано [58], что этот последний ион легко расщепляется на осколки С5, другими словами, эта реакция является обратимой. [19]
 |
Идеализированные структуры. [20] |
LiT и iLi1 I 2Sn v; последние ионы сами упорядочены в слое. [21]
С-О) 4А1 - и А1Н4 -, причем последний ион и является единственной атакующей частицей. [22]
Прохождение разряжающихся ионов через двойной электрический слой может встречать некоторые препятствия Для преодоления последних ионы должны подвергаться электрической активации в двойном слое. Это обуславливает особый вид поляризации, называемой актива-ционной. Не вдаваясь в механизм активационной поляризации, отметим лишь основные закономерности, которым она подчиняется. [23]
Возможно, что после разрыва молекул кислоты на ионы ОН - и NO з из последних ионов и молекул поверхностного окисла сразу образуются ионы Fe и NO -, и первые из них пере-содят в глубь раствора, а вторые входят во внешнюю обладку двойного электрического слоя. [24]
Из вышесказанного следует, что все количество ионов, подлежащих выделению на катоде, не может быть иолучено полностью, так сказать, до последнего иона. По мере выделения металла концентрация иона все время уменьшается, следовательно, по уравнению Нернста будет уменьшаться электродный потенциал данного металла. [25]
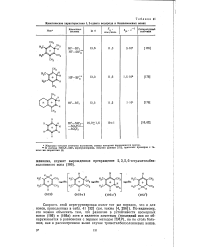 |
Кинетические характеристики 1 2-сдвига водорода в бензолониевых ионах. [26] |
По-видимому, это можно объяснить тем, что различие в устойчивости изомерных ионов ( 103) и ( ЮЗа) хотя и является заметным ( последний ион не обнаруживается в равновесии с первым методом ПМР), но не столь большое, как в рассмотренном выше случае триметилбензолониевых ионов. [27]
Реакция превосходна и специфична, потому что окраски, вызываемые ионами Fe2, Fe3, UOij 1 и Ti4 ( зеленая для двух первых и бурая и красная для двух последних ионов), исчезают в среде, сильно подкисленной азотной кислотой. [28]
В предыдущих соображениях мы всегда принимали, что скачок потенциала таких окислителей или восстановителей как раствор Fe / Fe % в превращении которых Н и ОН - не участвуют, не зависит от концентрации этих последних ионов и, следовательно, одинаков в кислом и в щелочном растворе при том условии, конечно, что концентрация их собственных ионов остается неизменной. [29]
При соединении электродов элемента проводником в цепи возникает ток, свободные электроны переходят на медную пластину, электрическое поле между цинковым электродом и электролитом ослабляется; при этом нарушается равновесие электрических и сторонних сил, и под влиянием последних ионы цинка снова переходят в раствор, а положительные ионы водорода приближаются к медной пластине, отнимают от нее свободные электроны и превращаются в нейтральные молекулы водорода. Медный электрод оказывается отделенным от электролита непроводящим слоем водорода. Это явление называется поляризацией элемента. [30]
Страницы: 1 2 3 4