Активность - щелочной металл
Cтраница 1
Активность щелочных металлов по отношению к различным веществам меняется по-разному. К кислороду самым большим сродством обладает литий и самым меньшим - цезий. [1]
Активность щелочных металлов по отношению к кислороду и фтору в подгруппе уменьшается сверху вниз, а по отношению к хлору, брому и иоду - увеличивается. [2]
Учет изменения активности щелочного металла с изменением его концентрации в амальгаме, а также отличие величины коэффициента переноса а от 0 5, приводят к несколько более сложным зависимостям, которые могут быть получены аналогичным путем. [3]
Известно, что активность щелочных металлов возрастает в ряду литий-натрий - калий, причем последний cnocodeH самовозгораться при нагревании на воздухе, поэтому от работы с ним пришлось отказаться. [4]
Данные об изменении коэффициентов активности щелочных металлов в ртути при добавке третьего металла приведены в табл. 2 и обсуждаются в гл. [5]
Активность этих элементов значительно ниже активности щелочных металлов. Это обусловлено особым расположением электронов в сих атомах. [6]
Активность этих элементов значительно ниже активности щелочных металлов. Это обусловлено особым расположением электронов в двух внешних слоях атома. [7]
Это правило безусловно проявляется также и в группе щелочных металлов; активность щелочных металлов заметно возрастает от лития к цезию. [8]
Небольшое число имеющихся в литературе количественных данных согласуется с представлениями о том, что активность щелочного металла в реакциях полимеризации зависит от степени его электроположительности. Так, Циглер [11] отмечает, что при полимеризации диолефинов натрий активнее лития. По данным [342], эффективность щелочных металлов полимеризации изопрена такова: цезий и натрий-калиевые сплавы активнее калия и рубидия, а последние более активны, чем натрий. Активность различных металлоорганических соединений данного щелочного металла, как показали Вудинг и Хиггинсон [362], увеличивается с ростом основности органического радикала. [9]
Помимо стеклянных электродов, предназначенных для измерения рН, выпускаются также стеклянные электроды для измерения активности щелочных металлов. [10]
Эта разница эквивалентна изменению величины изобарно-изотермического потенциала при переходе от щелочного металла к амальгаме с активностью щелочного металла в ней, равной единице. [11]
Таким образом, в общем случае потенциал любого стеклянного электрода обусловливается двумя величинами: активностью ионов водорода и активностью щелочного металла. [12]
Из уравнения (1.1) следует, что потенциал амальгамного электрода определяется не только активностью потенциало-определяющих ионов в растворе, но он также зависит, как это было впервые показано Тюриным [98-100], и от логарифма активности щелочного металла в амальгаме. [13]
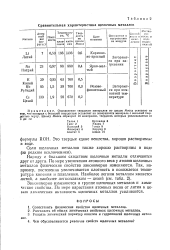 |
Сравнительная характеристика щелочных металлов. [14] |
Закономерно изменяются в группе щелочных металлов и химические свойства. По мере нарастания атомных весов от лития к це-химическая активность щелочных металлов усиливается. [15]
Страницы: 1 2