Трехзарядный ион - лантаноид
Cтраница 1
Трехзарядные ионы лантаноидов - элементов, относящихся к 4 / - типу, обладают электронной конфигурацией ( 18 пе -), которой свойствен явно выраженный поляризующий эффект. В связи с тем, что в последних, наряду с карбоксильной группой, имеются N-группы ( амино, нитрило), они с ионами лантаноидов образуют внутрикомплексные ( клешневидные) соединения. На свойстве ионов лантаноидов образовывать комплексные соединения с органическими кислотами основано их элюиро-вание из сорбционных слоев ионнообменных смол. [1]
Радиусы трехзарядных ионов лантаноидов постепенно уменьшаются с ростом атомного номера. [2]
Элюировямие трехзарядных ионов лантаноидов и актгшоидов с ионообменной смолы дауэкс-50 раствором а-оксиизобутирата аммония ( Seaborg G. [3]
Положение уровней трехзарядных ионов лантаноидов в кристаллической матрице гранатов было предметом многочисленных исследований [24], и следующий раздел посвящен обсуждению итогов наблюдения электронного КР для некоторых этих ионов; рассмотрены также теоретические положения, позволяющие установить правила отбора в электронных спектрах КР. [4]
При образовании трехзарядных ионов остальных лантаноидов наряду с повышением концентрации электронного газа до 2 эл / атом ( способствующей возрастанию энергии связи ионов, о чем можно судить, например, по повышению температур плавления при переходе от бария к лантану, от европия к гадолинию и от иттербия к лютецию) одновременно происходит сжатие внешних рв-оболочек их ионов. Это обстоятельство означает сокращение протяженности р-орбиталей, которые уже не перекрываются. Однако с повышением температуры энергия электронов на внешних р-уровнях возрастает и протяженность р-орбиталей увеличивается. Энергия же свободных электронов и, следовательно, энергия взаимодействия их с ионами существенно не изменяются. Таким образом, расширение р-орбиталей опережает увеличение межатомных расстояний, в области высоких температур наступает перекрытие р-орбиталей и возникает обменное направленное взаимодействие по осям прямоугольных координат. Это приводит к появлению объемноцентрированных кубических высокотемпературных модификаций, свойственных всем лантаноидам. Вследствие лантаноидного сжатия р6 - оболочек ионов появление объемноцентрированной модификации происходит при тем более высокой температуре, чем больше атомный номер лантаноида ( см. рис. 69, а), причем этот же фактор объясняет возрастание и их температур плавления от лантана до самария и от гадолиния до тулия и лютеция. [5]
Наиболее ярко люминесцируют трехзарядные ионы лантаноидов цериевой группы: самария, европия, гадолиния, тербия, диспрозия. Способность лантаноидов люминесцировать используется для их определения. [6]
Явление уменьшения радиусов трехзарядных ионов лантаноидов с ростом их атомного номера известно под названием лантаноидного сжатия. [7]
Химические свойства трехзарядных ионов актиноидов подобны свойствам трехзарядных ионов лантаноидов. Так, фториды осаждаются из растворов разбавленной азотной кислоты. Поскольку ионные радиусы обоих рядов элементов сравнимы, то наблюдается заметное сходство в образовании комплексных ионов, таких, как цитраты, а также в величинах констант комплексообразования. Разделение трехзарядных ионов лантаноидов и актиноидов на группы и их отделение друг от друга требует использования методов ионообменной хроматографии ( разд. [8]
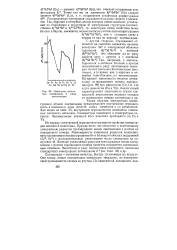 |
Изменение энтальпии атомизации в ряду лантаноидов. [9] |
Но наряду с внутренней периодичностью многие свойства лантаноидов меняются монотонно. Прежде всего это относится к постепенному уменьшению радиусов трехзарядных ионов лантаноидов с ростом их порядкового номера. Явление уменьшения радиусов трехзарядных ионов лантаноидов с ростом порядкового номера элемента называется лантаноидным сжатием. [10]
Другими словами, нарушение закона Бера связано с увеличением отношения ширины щели монохромато-ра к ширине полосы поглощения данного вещества. В случае сравнительно узких полос поглощения и небольших молярных коэффициентах погашения ( например, спектры поглощения трехзарядных ионов лантаноидов) значения F / могут оказаться достаточно большими и отклонения от закона Бера можно наблюдать и при малых раскрытиях щели. [11]
Для обнаружения неорганических и органических веществ в качественном анализе используют собственную люминесценцию. Из неорганических соединений в растворенном состоянии люминесцируют в ультрафиолетовом свете соли тяжелых металлов Т1, Sn2, Sb3, Pb2, Bi3, In3 и др. Наиболее ярко люминесцируют трехзарядные ионы лантаноидов цериевой группы: самария, ев ропия, гадолиния, тербия, диспрозия. [12]
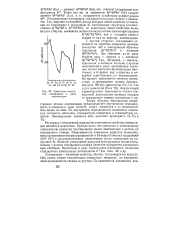 |
Изменение энтальпии атомизации в ряду лантаноидов. [13] |
Но наряду с внутренней периодичностью многие свойства лантаноидов меняются монотонно. Прежде всего это относится к постепенному уменьшению радиусов трехзарядных ионов лантаноидов с ростом их порядкового номера. Явление уменьшения радиусов трехзарядных ионов лантаноидов с ростом порядкового номера элемента называется лантаноидным сжатием. [14]
Факторы, определяющие устойчивость комплексов в зависимости от природы катиона. Если сравнить устойчивости комплексов, имеющих одинаковые лиганды и различные центральные катионы, то здесь также наблюдаются определенные закономерности. Для ионов непереходных элементов, а также для ионов переходных элементов, не имеющих d - электронов ( d), и для трехзарядных ионов лантаноидов стабильность комплексов возрастает по мере повышения заряда центрального катиона, а в случае одинаковых зарядов катионов - по мере уменьшения ионного радиуса. [15]
Страницы: 1 2