Мешающий ион - металл
Cтраница 1
Мешающие ионы металлов предварительно экстрагируют тем же реагентом, причем мышьяк ( V) при экстракции остается в водной фазе. [1]
Мешающие ионы металлов в анализируемом растворе предварительно удаляли электролизом в ячейке с отделенным анодом. [2]
Наиболее простым методом отделения мешающих ионов металлов является осаждение их карбонатом кальция или бария. Однако этот метод не всегда применим. [3]
При рН 10 прочные комплексы с ЭДТА образуют многие металлы различной природы, поэтому для получения специфической реакции на цинк необходимо удалить или замаскировать мешающие ионы металлов. [4]
Селективность метода может быть значительно повышена при использовании маскирующих агентов. Такими маскирующими агентами могут быть комплексующие агенты ( цианид, тартрат и ЭДТА), которые при добавлении к раствору пробы предотвращают реакцию между ок Сином и мешающим ионом металла. [5]
Имеющиеся для фотометрического определения кальция реагенты не обладают достаточной селективностью, поэтому в большинстве случаев необходимо предварительное отделение сопутствующих элементов. Осаждение не рекомендуется из-за адсорбции кальция осадком. Исключение представляет осаждение мешающих ионов металлов в виде сульфидов из кислого раствора. Отделение кальция от других щелочноземельных металлов осаждением в виде карбоната или оксалата требует многократного переосаждения [102], а при небольшом количестве кальция приводит к значительной его потере. Лучшим методом отделения кальция от сопутствующих элементов является экстракция. Для экстракции применяют 2 % - ный раствор оксина в хлороформе, содержащий 2 % н-бутиламина. [6]
Меркл и Хехт [120] приготовили силикагель, пропитанный триизооктиламином, образующим комплексы с ионами металлов. Туерлер и Хегл [ 120а ] использовали двузамещенную натриевую соль зтилен-диаминтетрауксусной кислоты для удерживания мешающих ионов металлов. [7]
Окислительно-восстановительный потенциал пары Pu ( III) - Pu ( IV) в 1 М НС1 равен 0 97 в; в 1 М НС1О4 - 0 98 ей в 1 М PbSCH - 0 75 в. Для фотометрического определения плутония ( IV) используют такие реагенты, как ализаринсульфо-нат натрия [33], который дает комплекс, имеющий при 530 ммк и рН 3 е9870, торон ( е 11 000 при 540 ммк) [34] и арсеназо I [35], который образует комплекс 1: 1 с е21 000 при 580 ммк в 0 1 М азотной кислоте. Pu ( III) ( при рН 5 5 - 6 5), Pu ( IV) и Pu ( VI) ( при рН 8 5 - 9 5) также образуют с арсеназо I окрашенные комплексы. Ни один из этих реагентов не является достаточно избирательным, так что необходимо предварительное отделение мешающих ионов металлов, а также некоторых анионов. [8]
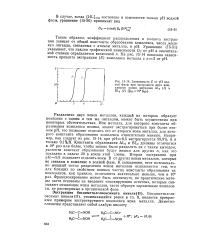 |
Зависимость Е от рН водной фазы при экстракции двух комплексов ионов металлов AL2 ( / и BL2 ( 2 [ р2А106 32в ]. [9] |
Разделение двух ионов металлов, каждый из которых образует комплекс с одним и тем же лигандом, может быть осуществимо при некоторых обстоятельствах. Ион металла, для которого константа образования комплекса велика, может экстрагироваться при более низком рН, что позволяет отделить его от второго иона металла, для которого константа образования комплекса относительно меньше. Константы образования AL2 и BL2 должны отличаться в 106 раз или более, чтобы можно было разделить их с таким выходом; разности констант образования будут иными для других п, как это показано в задаче 20 в конце этой главы. В от других ионов металлов, которые не связаны в комплекс в водной фазе. К сожалению, этот потенциально мощный метод разделения ионов металлов осложняется тем, что для близких по свойствам ионных частиц константы образования их комплексов, как правило, отличаются значительно меньше, чем в 10е раз. Фракционирование может быть достигнуто, но практические методы часто основаны на введении маскирующих агентов, которые свя-зывают мешающие ионы металлов, часто образуя заряженные комплексы, не растворимые в органической фазе. [10]
Метод имеет и другое преимущество, заключающееся в том, что мешающие хлорид-ионы автоматически удаляются. Избыток Ва2 - ионов не мешает. По-видимому, можно также проводить восстановление раствором аскорбата натрия. Восстановление железа проводят непосредственно перед добавлением раствора нитрата висмута. Согласно Риделю, мешающие ионы Hg и Sb легко удаляются осаждением их в виде сульфидов. Из остальных мешающих ионов металлов можно назвать только очень редко присутствующие в растворе In, Ga, Zr и Th. [11]
Страницы: 1