Многозарядный ион
Cтраница 2
Для многозарядных ионов следует учитывать кратность ионизации атомов. [16]
У многозарядных ионов ( S6) заряд ядра ( 16) намного превышает число электронов ( 10) и сильно стабилизирует электронную оболочку: такие ионы мало поляризуемы. У отрицательно заряженных ионов ( О2, F) положительный заряд ядра ( 8, 9) меньше числа электронов ( 10) и мало стабилизирует оболочку: такие ионы легко поляризуемы. [17]
Действие многозарядных ионов подробно изучал С. Он показал, что перезарядка поверхности вызывается адсорбцией не ионов поливалентных металлов, а продуктов гидролиза их солей. [18]
Для многозарядных ионов дополнительные трудности возникают из-за того, что специфическое взаимодействие ионов, предложенное Бренстедом, оказывает гораздо более сильное влияние на скорость реакции, чем изменение коэффициентов активности. Поэтому корреляция между lg ( / c / / c) и концентрацией многозарядного иона; противоположного по знаку иону, участвующему в реакции, соблюдается лучше, чем между lg ( / c / / co) иионной силой раствора. Это совершенно очевидно противоречит уравнению Бренстеда. [19]
В р-ре многозарядные ионы ( А1Э, Сг3, Ве2 и др.) и небольшие однозарядные ( 1л) достаточно прочно связывают ближайшие к ним молекулы воды, образуя аквака-тионы, напр. Кристаллогидраты солей обычно образуются в тех случаях, когда катионы в их кристаллич. [20]
Следовательно, многозарядные ионы перемещаются быстрее однозарядных. В результате многочисленных столкновений частиц с различными скоростями медленные компоненты ускоряются и приобретают дополнительную кинетическую энергию от быстрых. По результатам измерений можно судить о том, что этот процесс не заканчивается выравниванием скоростей и многозарядные ионы передают свою избыточную энергию однозарядным. [21]
При этом многозарядные ионы ( А1 3, Fe 3 и др.) способны не только снижать - потенциал, но и вызывать перезарядку - смену знака - потенциала за счет специфической адсорбции ионов. [22]
Как гидролизуются многозарядные ионы. [23]
Формы стабилизации многозарядных ионов в твердых телах в первую очередь зависят от матрицы, в которой происходит процесс. Например, в металлах железо после / С-захвата в 57Со стабилизируется в характерной для металлов форме нейтральных атомов. В соединениях железа и кобальта стабилизация, как правило, приводит к появлению Fe2 и Fe3; ни в одном соединении не отмечалось возникновения в мессбауэровских спектрах линий, связанных с зарядовыми состояниями железа, которые не были бы характерными для химии железа, / ( - захват в случае превращения 1251 в 125Те также приводит к стабилизации теллура в формах, характерных для макрохимии теллура. [24]
Дуговой масс-спектр многозарядных ионов отличается от искрового тем, что линии 1 -, 2 -, 3 - и 4-зарядных ионов необычно интенсивны, тогда как остальные едва видимы. Такой спектр с трудом поддается расшифровке. При получении масс-спектра в искровом разряде обычно пренебрегают многозарядными ионами, полагая, что они вносят незначительный и примерно одинаковый для всех элементов вклад в общий спектр. Для дугового спектра соотношение имеет обратный характер, поэтому следует учитывать вклад первых четырех состояний по заряд-ности, а также различные фотографические эффекты, связанные с наличием в нем ионов с высокими энергиями. Хотя вследствие высоких энергий в искровом источнике образование молекулярных ионов маловероятно, тем не менее примеси с высоким содержанием и элементы основы могут дать молекулярные ионы, что особенно характерно для элементов IV группы. [25]
Каталитическое действие многозарядных ионов в электрохимическом восстановлении перекиси водорода во многом аналогично их действию в обычных окислительно-восстановительных реакциях и обусловлено образованием перекисных комплексов. [26]
В растворах многозарядных ионов структурирование растворителя становится столь значительным, что они приобретают свойства, присущие кристаллосольватам. Наоборот, ионы, обладающие деструктурирующим действием ( К, NO3 и др.), оказывают разрыхляющее влияние на приионную зону сольватов. Последнее делает понятным отсутствие высокозарядных ионов в водных растворах. Так, растворение солей Со3 не приводит к образованию Со34 ( р) - происходит окислительно-восстановительный процесс, сопровождающийся выделением кислорода. [27]
Избирательность сорбции многозарядных ионов играет существенную роль при извлечении многих органических соединений, содержащих несколько основных или кислотных групп. [28]
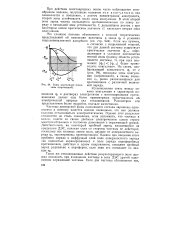 |
Зоны коагуляции ( показаны штриховкой. [29] |
При действии многозарядных ионов часто наблюдается своеобразное явление, получившее название зон коагуляции; оно заключается - в появлении, с ростом концентрации электролита, второй зоны устойчивости после зоны коагуляции. В этой второй зоне заряд частиц оказывается противоположным по знаку заряду в начальной зоне устойчивости. С дальнейшим ростом с при некотором новом критическом значении с к наступает вторая зона коагуляции. [30]
Страницы: 1 2 3 4