Природный гелий
Cтраница 1
Природный гелий состоит из стабильных изотопов 8Не и 4Не, последний преобладает. [1]
Природный гелий состоит из двух изотопов - 3Не и 4Не - и представляет собой смесь радиогенного ( особенно 4Не) и первичного ( 3Не и 4 Не) газов. Главным источником4Не на Земле являются изотопы урана и тория. Кроме определения изотопных отношений 3Не / 4Не [33], при гидрогеологических исследованиях изучают распределения концентраций гелия в природных водах, т.е. используют водногелиевую съемку. [2]
Легкий изотоп гелия Не3 с атомной массой 3, находится в природном гелии, в количестве примерно равном одной части на миллион частей обычного гелия Не4, имеющего атомную массу, равную четырем. Hes также может быть получен искусственным путем в атомных реакторах, в частности, из лития. Легкий гелий сжижается при еще более низкой температуре ( 3 195 К), чем Не; он не переходит в сверхтекучее состояние вплоть до температуры 0 001 К, однако растворы Не3 и Не при некоторых соотношениях между компонентами обладают сверхтекучестью. Свойства растворов Не3 - Не4 используются в некоторых системах особо глубокого охлаждения. [3]
Оказалось также, как нашли Нир и Алдрич [152], что содержание легкого изотопа гелия Не3 в природном гелии может изменяться в сотни раз в зависимости от его происхождения. Отношение Не3: Не4 в воздухе равно 1 2 - 10 - 6, а в природном газе из скважин оно падает в десять и более раз. [4]
В заключение этого короткого обзора свойств гелия II я хочу вернуться к началу статьи и исправить ошибочное представление, которое я, возможно, здесь создал. Природный гелий состоит из почти чистого гелия 4 и все, что было сказано выше, относится к этому изотопу. [5]
Опыт был так продуман, чтобы гарантировать невозможность проникновения в вакуумную аппаратуру природного гелия из воздуха. Панет и Петере получили положительные результаты, то есть обнаружили гелий. [6]
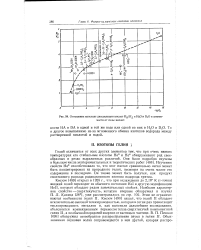 |
Отношение констант диссоциации кислот Кн / Ка в Н2О и D2O в зависимости от силы кислот. [7] |
Гелий отличается от всех других элементов тем, что при очень низких температурах его стабильные изотопы Не3 и Не4 обнаруживают ряд своеобразных и резко выраженных различий. Изучению свойств Не3 способствовало то, что этот изотоп сравнительно легко может быть концентрирован из природного гелия, несмотря на очень малое его содержание в последнем. Он также может быть получен, как продукт спонтанного распада радиоактивного изотопа водорода трития. [8]
Нейтральный атом гелия имеет также два электрона. Гелий обнаружен в месторождениях некоторых природных газов, и его получают в качестве побочного продукта. Источники природного гелия встречаются очень редко. [9]
Гелий, как и большинство элементов, имеет изотопы. Два из них устойчивы и потому находятся в природном газе. Однако фактически весь природный гелий состоит из изотопа Не4, а Не3 - лишь ничтожная добавка к нему. Долгое время он был не только главным, а единственным среди гелиев объектом исследования ( тем более, что легкий изотоп впервые обнаружили в 1939 году), и теория сверхтекучести построена именно для пего. [10]
Гелий, как и большинство элементов, имеет изотопы. Два из них устойчивы и потому находятся в природном газе. Однако фактически весь природный гелий состоит из изотопа Не4, а Не3 - лишь ничтожная добавка к нему. Долгое время он был не только главным, а единственным среди гелиев объектом исследования ( тем более, что легкий изотоп впервые обнаружили в 1939 году), и теория сверхтекучести построена именно для него. [11]
 |
Прибор для разделения изотопов гелия путем сверхтекучести.| Прибор для разделения изотопов гелия путем термомеханиче-ского эффекта. [12] |
В работе Б. Н. Есельсона и Б. Г. Лазарева [ П ] разделение изотопов гелия было значительно усовершенствовано и достигнуты успехи, далеко превосходящие полученные ранее результаты. Для начального концентрирования применено видоизменение описанного выше метода, основанного на термомеханическом эффекте. Этим путем было достигнуто обогащение природного гелия изотопом Не3 в 200 раз при производительности до 2 л концентрата за одну операцию. Вторичное его концентрирование в таком же приборе меньших размеров дало обогащение еще в 12 раз. [13]
Тритий относится к числу искусственно-радиоактивных веществ; он распадается с периодом полураспада около 12 лет, испуская электроны. В результате распада трития образуется ядро с массовым числом 3 и зарядом 2 - легкий изотоп гелия 2Не3, состоящий из двух протонов и нейтрона. Этот изотоп устойчив и содержится в очень малой пропорции в природном гелии. [14]
Тритий относится к числу искусственно-радиоактивных веществ; он распадается с периодом полураспада около 12 лет, испуская электроны. В результате распада трития образуется ядро с массовым числом 3 и зарядом 2 - легкий изотоп гелия Не, состоящий из двух протонов и нейтрона. Этот изотоп устойчив и содержится в очень малой пропорции в природном гелии. Ядро основного изотопа гелия Не ( а-частица) образуется добавлением еще одного нейтрона, oc - частица содержит, таким образом, два протона и два нейтрона. [15]
Страницы: 1 2