Однозарядный ион
Cтраница 2
Каждый однозарядный ион независимо от его природы получает или отдает 1 электрон, и для выделения 1 моль любого одновалентного металла требуются одинаковые количества электричества. Для выделения 1 моль любого двухвалентного металла также требуются одинаковые количества электричества, но в два раза больше, чем для одновалентного металла. [16]
Ускоряем однозарядные ионы натрия, пропуская их через разность электрических потенциалов 90 В. [17]
 |
Первая группа периодической системы. [18] |
Однако положительные однозарядные ионы этих элементов, в виде которых все они ( кроме водорода) большей частью содержатся в соединениях, различаются по числу электронов на внешнем уровне. Ион водорода Н представляет собой ядро атома, полностью лишенное электронной оболочки; ион лития Li имеет два электрона, ионы натрия, калия, рубидия, цезия и франция содержат на внешнем уровне по 8 электронов, а однозарядные ионы меди, серебра и золота - по 18 электронов. [19]
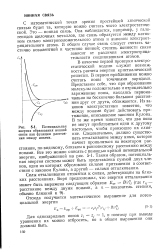 |
Потенциальная энергия образования ионной связи как функция расстояния между ионами. [20] |
Для однозарядных ионов г - z - t 1, и поэтому при выводе уравнения их можно отбросить, но в общем выражении они должны быть. [21]
Из однозарядных ионов ион лития наименее охотно адсорбируется, затем следуют натрий и калий ( которые ведут себя примерно одинаково) и, наконец, серебро. Из многовалентных металлических катионов алюминий и торий адсорбируются наиболее сильно. Это следует из того факта, что при очень низкой концентрации они меняют знак заряда золя кремнезема из отрицательного на положительный. [22]
Энергия однозарядного иона в воде также уменьшается в 81 раз по сравнению с энергией в вакууме. [23]
Для однозарядных ионов; у многозарядны. [24]
Среди однозарядных ионов наиболее устойчивые комплексы с Ри4 образует фторид-ион. [25]
Для однозарядных ионов г - г - 1, и поэтому при выводе уравнения их можно отбросить, но в конечном выражении они должны быть. [26]
Для однозарядных ионов z, Zj 1, и поэтому при выводе уравнения их можно отбросить, но в общем выражении они должны быть. [27]
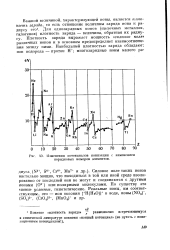 |
Изменения потенциалов ионизации с изменением порядковых номеров элементов. [28] |
Для однозарядных ионов ( щелочных металлов, галогенов) плотность заряда - величина, обратная их радиусу. Плотность заряда выражает мощность силового поля - различных ионов и в основном предопределяет взаимоотношения между ними. [29]
Заряд однозарядного иона соответствует заряду электрона, равному 4 8 - 10 - ед. [30]
Страницы: 1 2 3 4