Гельд
Cтраница 1
Гельд [3] указывает на возможность другого механизма, заключающегося во взаимодействии между компонентами твердой и жидкой фаз. Иною [4] утверждает, что СаО и С перед взаимодействием образуют твердый раствор. Этот процесс является обратимым; равновесное давление [5] паров кальция при 1100 С равно 0 001 мм рт. ст., при 1300 С 0 04 мм рт. ст. и при 1500 - С 0 7 мм рт. ст. Высокое парциальное давление СО тормозит прямую реакцию. Энергия активации прямой реакции ( при давлении 2 - 3 мм рт. ст., при котором не происходит последующего образования СаС2 [1, 6, 7]) зависит от природы исходных СаО и С. [1]
Гельд и Кочнев дают ( 1300 С) & F 32 500 кал / моль. Но Кубашевский и Эванс, оперируя данными советских авторов, приводят несколько иную величину 31100 кал. [2]
Гельд с сотрудниками [257] показал, что восстановители кремнезема располагаются по своему действию в следующий убывающий ряд: газообразный кремний, твердый углерод, жидкий кремний, твердый кремний, расплавленный ферросилиций, твердый ферросилиций, карборунд. Скорость восстановления кремнезема в вакууме при температуре ИЗО-1370 кремнием и ферросилицием почти одинакова, а карборундом и углеродом - значительно меньше. [3]
 |
Давление пара над твердой SiO ( но Гюнтеру.| Величины постоянных в уравнении давления пара моно. [4] |
Данные Гельда и Кочнева сохранили свое значение и до настоящего времени. [5]
Исследованиями Гельда [29, 43, 46], Кайнарского и Карякина [47], Марон и Микулинского [48] и других авторов показано большое значение газовой и жидкой фаз в процессах получения карбида кремния и карбида кальция. [6]
Есин и Гельд такого вывода, конечно, не сделали. [7]
Есин и Гельд [4] для объяснения непрекращающегося каталитического воздействия кристаллов на распад окиси углерода после обильного отложения сажи выдвинули схему механизма, согласно которой адсорбцию и расщепление молекул СО ведут в этих условиях микрокристаллические образования сажи. Отщепляющийся кислород мигрирует через решетку графита на обнаженные участки железной поверхности, откуда снимается молекулами СО, атакующими эти участки из газовой фазы. [8]
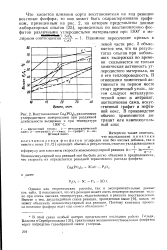 |
Восстановление Са3 ( РО4 2 различными углеродистыми материалами при различной длительности выдержки и при температуре. [9] |
В этой связи особый интерес представляет последняя работа Гельда, Власова и Серебренникова [33], трактующая механизм восстановления фосфатов через посредство газообразной окиси углерода. [10]
На рис. 90 показаны такие изотермы, полученные Гельдом и Самохваловым [79 ] при адсорбции лаурата натрия на сульфате бария. [11]
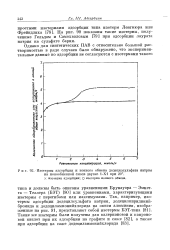 |
Изотермы адсорбции и ионного обмена додецилсульфата натрия на ионообменной смоле дауэкс 1 - Х1 при 20. X изотерма адсорбции. О изотерма ионного обмена. [12] |
На рис. 90 показаны такие изотермы, полученные Гельдом и Самохваловым [79] при адсорбции лаурата натрия на сульфате бария. [13]
Анализ большого ряда экспериментальных работ по опре-делению величины теплового эффекта образования окиси хрома из металлического хрома и кислорода имеется в монографии Гельда и Есина [27], которые приводят в качестве наиболее вероятного значения теплового эффекта реакции образования окиси хрома в стандартных условиях величину ДЯ298 - 1 125 800 2500 дж. [14]
Предста вления Таммана и Зворыкина [14], Баукло и других [15] о механизме восстановления окислов твердым углеродом, как показали Банков и Тумарев [16], Гельд, Есин [17, 18] и другие исследователи, не соответствуют фактическим данным об этом процессе. [15]
Страницы: 1 2