Гемоглобин - кровь
Cтраница 1
Гемоглобин крови имеет в 200 - 250 раз более высокое сродство к СО, чем к О. При 60 % - ном содержания карбоксигемоглобина парциальное давление кислорода в тканях тела человека составляет 5 - 10 мм рт.ст., что является критическим условием. Субъективные признаки интоксикации возникают при концентрации карбоксигемоглобина в крови 40 % и проявляются головной болью, усталостью. В атом состоянии даже небольшое физическое напряжение, связанное, например, с попыткой покинуть очаг пожара, может привести к потере сознания. Авторы приходят к выводу о том, что продолжительность контакта с продуктами горения должна быть максимально сокращена ввиду отрицательного воздействия на организм человека всех форм продуктов горения. [1]
Гемоглобин крови обладает активностью пероксидазы и каталитически ускоряет окисление бензидина перекисью водорода в бензидиновую синь. [2]
Гемоглобин крови состоит из комплексного гетероциклического соединения, называемого пигментом или простетической группой; и бесцветного белкового вещества или глобина. Окрашенная часть, называемая гемпном, дает при удалении пз нее железа порфирин. Существует много порфпринов, полученных из других источников, Ппрфирин крови назван протопорфирин или оопорфирин для отличия его от других порфиринов. Нормально железо гемоглобина составляет около 55 % всего железа организма. Железо в гемоглобине находится в закисной форме. Оно связывает порфирин и белок, образуя металлопорфирин - белковый комплекс. [3]
Гемоглобин крови состоит из двух субединиц ( при молекулярном весе суммарной частицы 68 000), соединенных слабыми, по-видимому, солевыми связями. Каждая из двух субединиц состоит из двух полипептидных цепей, связанных также ионными связями. При элюции концентрация буфера плавно увеличивается в 10 раз ( градиентная элюция) и в разные моменты времени с ионообменника смываются оба фрагмента гемоглобина А и В, и мы получаем их в чистом виде. Их дальнейшее разделение на отдельные пептидные цепи может быть осуществлено в щелочной среде. [4]
Гемоглобин крови служит разделяющим агентом благодаря способности обратимо реагировать с кислородом с образованием окси-гемоглобина. Для приготовления неподвижной фазы к огнеупорному кирпичу С-22 ( 120 / 170 или 170 / 200 меш) медленно добавляют кровь человека или животного из расчета 0 5 мл на 1 г. Перемешивание продолжают до тех пор, пока масса не станет однородной, после чего подвижный порошок засыпают в U-сбразную стеклянную трубку. Чтобы удалить кислород, колонку продувают гелием и кровь хранят до употребления в холодильнике в атмосфере гелия. На колонке длиной 2 м при температуре 30 - 40 получают прекрасное отделение кислорода от азота с почти симметричным пиком кислорода. При 20 - 25 результаты не столь хороши, а при 10 разделения совсем не происходит. При скорости потока газа-носителя менее 8 мл / мин часть кислорода оказывается необратимо связанной. [5]
Гемоглобин крови представляет собой железный комплекс одного из порфиринов ( протопорфирина) в связи с белковым веществом - глобином. [6]
Переводит гемоглобин крови в метгемогло-бин и вторично вызывает распад красных кровяных телец. Действует на нервную систему угнетающе; в больших дозах вызывает судороги, затем паралич и смерть от остановки дыхания. [7]
Переводит гемоглобин крови в метгемогло-бин и вторично вызывает распад кратных кровяных телец. Действует на нервную систему угнетающе; в больших дозах вызывает судороги, затем паралич и смерть от остановки дыхания. Смертельные дозы: для кроликов ( при даче внутрь) 0 075 - 0 01 г ( в виде хлористоводородной соли), для собак - 0 2 - 0 3 г. В производственных условиях отравления не описывались. [8]
Роль гемоглобина крови и хлорофилла в растениях исключительно велика. Поэтому железо совершенно необходимо для жизни человека, животных и растений. [9]
С гемоглобином крови СО связывается прочнее, чем кислород, тем самым блокирует перенос кислорода в организме. [10]
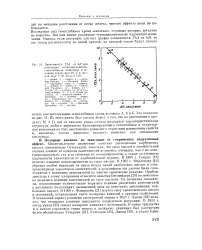 |
Зависимость T & S от Ml для ионизации мотагемоглобипов, гемоглобинов животных и человека в воде при. 20 С и ионной силе 0 05 моль / л. [11] |
Исследован ряд гемоглобинов крови животных, строение которых детально не известно. Все они имеют различные термодинамические параметры ионизации. [12]
Дыхательная функция гемоглобина крови подробно рассматривается в курсе физиологии. Здесь следует указать на уникальную роль гемоглобина в траспорте кислорода от легких к тканям и диоксида углерода от тканей к легким. Это элементарное проявление жизни-дыхание, хотя и выглядит простым, основано на взаимодействии многих типов атомов в гигантской молекуле гемоглобина. Подсчитано, что в одном эритроците содержится около 340000000 молекул гемоглобина, каждая из которых состоит примерно из 103 атомов С, Н, О, N, S и 4 атомов железа. [13]
За исключением гемоглобина крови, меланины являются единственными пигментами, которые синтезируются и широко используются млекопитающими. Они также представляют собой обычные пигменты оперения птиц. Черная кожа, волосы, шерсть и перья окрашены эумеланинами. Желтый, рыжий и коричневый цвет волос и шерсти обусловлены феомеланинами, которые служат также пигментами в коричневых, а в некоторых случаях в желтых и красных перьях. Пигментами желтых и красных перьев могут быть и каротиноиды ( гл. Феомела-нины найдены только у млекопитающих и у птиц, тогда как эумеланины широко встречаются также у рыб и беспозвоночных. Однако в некоторых случаях темная окраска у ряда насекомых и других членистоногих вызывается не меланинами, как думали раньше, а оммохромами ( гл. [14]
В составе гемоглобина гем крови посредством центрального иона железа связывает кислород и переносит его из легких к мышцам. Отдав кислород, гемоглобин использует аминогруппы для связывания молекул СО2 и переноса их в легкие. [15]
Страницы: 1 2 3 4