Гемоглобин - плод
Cтраница 1
Гемоглобин плода имеет более высокое сродство к кислороду, чем гемоглобин взрослого человека, и поэтому эффективность газообмена повышается. Диоксид углерода, представляющий собой конечный продукт обмена при аэробном дыхании, диффундирует в противоположном направлении. [1]
Гемоглобин плода, так называемый Hb-F, несколько отличается и по своему химическому строению от гемоглобина взрослых людей ( стр. [2]
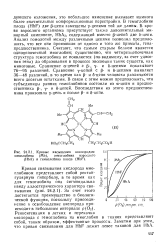 |
Кривые насыщения кислородом 100 миоглобина ( Mb, гемоглобина взрослого ( НЬА и гемоглобина плода ( HbF. [3] |
В гемоглобине плода ( HbF) две р-цепи замещены у-цепями той же длины. В крови взрослого организма присутствует также дополнительный минорный компонент, НЬАз, содержащий вместо р-цепей две 6-цепи. [4]
При смешивании гемоглобина плода HbF с меченым НЬА при рН4 и последующей нейтрализации раствора образуется гемоглобин плода с меткой в а-цепи. Очевидно, а-цепи, содержащиеся в НЬА и в HbF, идентичны. Индивидуумы, гомозиготные по гену HbS, должны иметь нормальный HbF. Вместе с тем у индивидуумов, гемоглобин которых имеет аномалии в а-цепях, можно ожидать аномалий в гемоглобине плода. Последовательности аминокислот в у - и р-цепях более сходны друг с другом, чем с последовательностью в а-цепи. [5]
При смешивании гемоглобина плода HbF с меченым НЬА при рН4 и последующей нейтрализации раствора образуется гемоглобин плода с меткой в а-цепи. Очевидно, а-цепи, содержащиеся в НЬА и в HbF, идентичны. Индивидуумы, гомозиготные по гену HbS, должны иметь нормальный HbF. Вместе с тем у индивидуумов, гемоглобин которых имеет аномалии в а-цепях, можно ожидать аномалий в гемоглобине плода. Последовательности аминокислот в у - и р-цепях более сходны друг с другом, чем с последовательностью в а-цепи. [6]
У плацентарных позвоночных плоду приходится конкурировать за О2 с тканями матери. Кровь плода должна извлекать кислород из материнской крови через плацентарный барьер, и эту задачу намного облегчает то, что эритроциты плода содержат особый вариант гемоглобина ( гемоглобин плода), обладающий большим сродством к О2, чем гемоглобин взрослого животного. Таким образом, гемоглобин плода, который по сродству к О2 занимает промежуточное положение между гемоглобином взрослого типа и окислительными ферментами в тканях плода, функционирует аналогично миоглобину в том смысле, что он тоже служит посредником в передаче кислорода от крови дышащим тканям. [7]
У плацентарных позвоночных плоду приходится конкурировать за О2 с тканями матери. Кровь плода должна извлекать кислород из материнской крови через плацентарный барьер, и эту задачу намного облегчает то, что эритроциты плода содержат особый вариант гемоглобина ( гемоглобин плода), обладающий большим сродством к О2, чем гемоглобин взрослого животного. Таким образом, гемоглобин плода, который по сродству к О2 занимает промежуточное положение между гемоглобином взрослого типа и окислительными ферментами в тканях плода, функционирует аналогично миоглобину в том смысле, что он тоже служит посредником в передаче кислорода от крови дышащим тканям. [8]
В крови зародыша на ранних стадиях его развития присутствует гемоглобин третьего типа. Зародышевый гемоглобин F обладает более высоким сродством к кислороду, чем гемоглобин А взрослых людей. Благодаря этому возможен оптимальный перенос кислорода от гемоглобина А матери к гемоглобину F плода. [9]
Дана зависимость насыщения гемоглобина ( НЬ) кислородом при рН 7 2 от концентрации свободного кислорода. Концентрации 02 в капиллярах легких ( 125 мкМ) н в капиллярах тканей, потребляющих О2 ( 50 мкМ), зафиксированы в узких пределах. Кривая а: в отсутствие дифосфоглицерата ( ДФГ) гемоглобин насыщается Ог в легких, но не может доставлять его к тканям. Кривые бив: поскольку гемоглобин плода ( кривая в) имеет более низкое сродство к ДФГ. [10]
При смешивании гемоглобина плода HbF с меченым НЬА при рН4 и последующей нейтрализации раствора образуется гемоглобин плода с меткой в а-цепи. Очевидно, а-цепи, содержащиеся в НЬА и в HbF, идентичны. Индивидуумы, гомозиготные по гену HbS, должны иметь нормальный HbF. Вместе с тем у индивидуумов, гемоглобин которых имеет аномалии в а-цепях, можно ожидать аномалий в гемоглобине плода. Последовательности аминокислот в у - и р-цепях более сходны друг с другом, чем с последовательностью в а-цепи. [11]
В 1949 г. Полинг, Итано, Сэнгер и Уэллс обнаружили, что гемоглобин больных серповидноклеточной анемией, HbS, отличается по своей электрофоретической подвижности от нормального гемоглобина человека, НЬА. Это исследование, в котором было обнаружено различие зарядов двух форм молекул гемоглобина, положило начало изучению молекулярных болезней крови. Генетики установили, что серповидноклеточная анемия наследуется по простым менделевским законам. Индивидуумы, гомозиготные по гену HbS, обычно умирают в раннем возрасте. В их крови часто сохраняется значительное количество гемоглобина плода, У индивидуумов, гетерозиготных по этому гену, содержится примерно 40 % HbS. [12]
III указывалось, что первичная структура некоторых полипептидных гормонов ( в частности, вазопрессина и меланоцитстимулирующего гормона) у разных биологических видов не вполне одинакова. Такая же видовая специфичность наблюдается и у белков. В препаратах цитохрома с, выделенных от разных видов, также были обнаружены индивидуальные различия, определяющиеся природой аминокислот в ключевом пептидном сегменте. Помимо этих вариаций, обусловленных видовой специфичностью, встречаются также и различия в белках одного и того же вида, возникшие в результате мутаций. Большинство сведений о влиянии мутаций на структуру белка почерпнуто нами из прекрасных работ Ингрэма. Ингрэм и его сотрудники показали, что нормальный гемоглобин взрослого человека и гемоглобин больных таким наследственным заболеванием, как серповидноклеточная анемия, отличаются только тем, что в определенном положении р-цепи остаток глутаминовой кислоты в аномальном гемоглобине заменен валином. Напомним, что молекула гемоглобина состоит из двух пар идентичных цепей: а - и р-цепей в гемоглобине взрослого человека или ос - и у-цепей в гемоглобине плода. [13]
Гемоглобин - олигомерный белок, который состоит из четырех субъединиц. Субъединицы а и р в третичной структуре весьма напоминают молекулу миоглобина. При связывании первой молекулы О2 происходит втягивание атома железа в плоскость тема. В итоге кривая связывания кислорода гемоглобина имеет S-образный вид. Такой тип зависимости определяется кооперативным ( совместным) действием всех субъединиц в интересах целой молекулы гемоглобина. Очевидно, что оксигемоглобин будет отдавать О2, а миоглобин его связывать. Сродство гемоглобина к О2 характеризуется величиной Р5о - значение / Ю2, при котором наблюдается полунасыщение гемоглобина кислородом. Значение Р50 всегда превышает значение / Ю2 в периферических тканях. Например, Р50 для HbAj составляет 26 мм рт. ст., а для фетального HbF - 20 мм рт. ст. Благодаря этой разнице гемоглобин F плода отбирает кислород у НЬА ( плацентарной крови матери. После рождения HbF должен утратить свою функцию, так как, обладая более высоким сродством к кислороду, он хуже освобождает его в тканях. [14]
Страницы: 1