Геометрия - радикал
Cтраница 1
Геометрия радикала РН3С - ( 49) представляет особый интерес, так как она прекрасно иллюстрирует стабилизацию благодаря эффективной делокализации неспаренного электрона. Максимальная стабилизация могла бы быть, однако, достигнута лишь тогда, когда все три бензольных кольца могли бы располагаться в одной плоскости [ ( 49а) ], так как только в этой конформации р-орбиталь центрального атома углерода может взаимодействовать одинаково и в максимальной степени с л-орбитальной системой каждого из трех ядер. В действительности триарилме-тильные радикалы, как было показано спектроскопическими и рентгеноструктурными методами, имеют форму пропеллера ( 496), причем бензольные кольца находятся под углом около 30 к общей плоскости. [1]
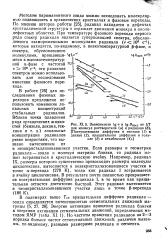 |
Зависимости lg v и lg 0ПОСТ от 1 / Т для молекул растворителя ( а и радикала ( б. [ Поступательная диффузия в гептане ( / н декане ( 2, вращательная диффузия в толуоле ( 3 и этилбензоле ( 4. ]. [2] |
Если размеры и геометрия радикала - зонда и молекул матрицы близки, то радикал может встраиваться в кристаллическую ячейку. Например, радикал IX, размеры которого существенно превосходят размеры молекулы циклогексана, вытесняется в незякристаллизовавшиеся участки в точке а-перехода ( 278 К), тогда как радикал I встраивается в ячейку циклогексана. В результате почти полностью прекращается поступательная диффузия радикала I, в то время как вращательная остается достаточно быстрой. [3]
Дает ли этот факт возможность сделать выбор для геометрии радикала. [4]
Во-вторых, альдиминоксилы существуют в виде двух достаточно устойчивых изомеров - сын и анти, и константы СТВ заметно зависят от геометрии радикала. [5]
По мнению авторов работы [27], эта неэквивалентность вызвана стерическим взаимодействием между кольцевыми протонами и заместителями в обеих кольцах, искажающим геометрию радикала, в результате которого изменяется распределение спиновой плотности. [6]
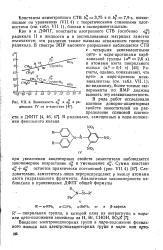 |
Зависимость aa и ав в ра - влияние донорно-акцепторных дикалах IV от а-констант. свойств заместителей на рас. [7] |
Как и в ДФПГ, константы изотропного СТВ ( особенно аУ) радикала II в жидкости и в застеклованных матрицах заметно отличаются; эти различия также вызваны искажением геометрии радикала. [8]
 |
Рацемизация при реакции, протекающей через стадию образования свободных радикалов. [9] |
Следует ясно представлять себе, что потеря стереохимической идентичности, хотя и согласуется с плоским строением радикала, но не обязательно требует такого строения. Более подробные сведения относительно преимущественной геометрии радикалов можно получить, изучая легкость их образования в тех случаях, когда либо они вынуждены быть плоскими, либо когда встречаются препятствия на этом пути. [10]
При таком анализе спектров не учитывается анизотропия g - тензора и предполагается, что изотропное СТВ в растворе и в замороженных матрицах одинаково. Однако матрица может искажать геометрию радикала, поэтому этот способ определения анизотропной части СТВ следует рассматривать лишь как оценочный, ориентировочный. Более строгий анализ заключается в построении теоретических спектров и подборе параметров ( компонент тензора СТВ и g - тензора), при которых экспериментальные спектры радикалов в стеклах совпадают с теоретическими. [11]
Уменьшение константы сверхтонкого взаимодействия в SiH3 рассматривалось в работе [26] на основе допущения о том, что радикалы SiH3 имеют слегка пирамидальную конфигурацию. Предполагается, что такое изменение геометрии радикала приводит первоначально к уменьшению величины сверхтонкого взаимодействия с протоном вследствие возникновения положительного вклада при изгибании радикала. Данный эффект должен быть противоположным отрицательному взаимодействию в плоском радикале. Этот вопрос рассмотрен подробно в гл. II, но до сих пор неизвестно, является ли взаимодействие с протоном в SiH3 положительным или отрицательным. [12]
Имеются, конечно, и усложняющие обстоятельства. Если электроотрицательность атома В достаточно велика, изменение злектроотрицательности атома А будет приводить к пренебрежимо малым изменениям геометрии радикала. В этом случае конфигурация радикала определяется в основном электроотрицательностью атома В. Схематической иллюстрацией данной точки зрения служит рис. VII. На рисунке показано изменение валентного угла ср в зависимости от электроотрицательности / д атома А для двух случаев - большой и малой электроотрицательности ( В атома В. [13]
 |
Спектр ЭПР этильного радикала со схематической диаграммой и интерпретацией спектра. [14] |
Константы сверхтонкого расщепления в замещенных алкиль-ных радикалах чувствительны к способности заместителей делока-лизовать неспаренный электрон. Так, протонные константы расщепления в радикалах типа СН2Х и - СНХ2 ( где X OR, CN, COR, COOR, Me) меньше, чем константы расщепления в метиль-ном радикале, если, конечно, геометрия сравниваемых радикалов одинакова. [15]
Страницы: 1 2