Гибридизация - орбиталь
Cтраница 2
Гибридизация орбиталей валентных электронов характерна не только для соединений углерода. [16]
Гибридизацией орбиталей какого атома она объясняется. [17]
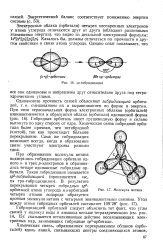 |
Молекула метана. [18] |
Гибридизацией орбиталей следует объяснить тот факт, что углы связей у молекул воды и аммиака меньше тетраэдрического ( см. рис. 14, 15): сказывается отталкивающее действие несвязывающих электронных пар, занимающих гибридные 5 / з3 - орбитали. [19]
При гибридизации орбиталей одного s - и двух р-электронов атома В возникают три гибридные орбитали, расположенные в одной плоскости под углом 120, которые, перекрываясь с орбиталями р-электронов атома галогена, образуют плоскую молекулу ВХ3 - sp3 - гибридизация. [20]
 |
Пронод ( вдоль слоев, образе. [21] |
Происходит гибридизация орбиталей между л - электронами атомов углерода в графите и валентными электронами легирующих примесей. [22]
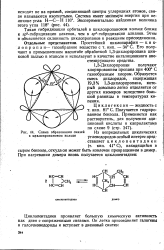 |
Схема образования связей в циклопропановом кольце. [23] |
Такая гибридизация орбиталей в циклопропановом кольце ближе к р2 - гибридизации алкенов, чем к вр3 - гибридизации алканов. Этим и объясняется склонность циклопропанов к реакциям присоединения. Его получают в промышленном масштабе обработкой 1 3-дихлорпропана цинковой пылью в этаноле и используют в качестве ингаляционного анестезирующего средства. [24]
При гибридизации орбиталей связи направлены таким образом, что обеспечивается максимально возможное удаление их друг от друга. Так, при тригональной плоской конфигурации достигается наибольшее удаление, возможное для трех связей; тетраэдрическая конфигурация четырех связей также обеспечивает максимальное удаление орбиталей; то же самое происходит при sp - гибридизации двух орбиталей ( угол 180) и в системах с 5 или 6 связями при sp3d - и 5р3 2-гибридизации. Взаимное отталкивание такого типа происходит не только между связывающими орбиталями, но и между связывающими и несвязывающими заполненными орбиталями, занятыми неподеленными парами электронов. Таким образом, реальная ориентация связей может зависеть от числа заполненных связывающих и несвязывающих орбиталей. В двухвалентном кислороде две р-ор-битали, участвующие в образовании связей, отталкиваются третьей 2р - орбиталыо, на которой находится неподеленная пара электронов, или несвязывающей гибридизованной sp - орбиталью. Другие элементы в этом плане будут рассмотрены позднее. [25]
Характер гибридизации орбиталей неподеленных пар кислорода в карбонильной группе однозначно не определен. Однако обосновано предположение, что одна орбиталь имеет р-характер, а вторая - больший s - характер. В частности, можно Принять [43, 44], что вторая неподеленная пара занимает 2spz ( О) - орбиталь. Эти электроны более прочно связаны с ядром, чем 2ру - электроны, поэтому соответствующие им переходы расположены в более коротковолновой области. [26]
Так как гибридизация орбиталей уже была описана в гл. [27]
Идея о гибридизации орбиталей связана с выводом о том, что гибридизованные орбитали имеют строго определенное направление в пространстве, отличное от направлений исходных орбиталей. Тетраэдрическая симметрия атома углерода хорошо объясняется с этой точки зрения. Поэтому геометрия молекулы должна зависеть от геометрии гибридных орбиталей составляющих ее атомов. [28]
Так как гибридизация орбиталей была описана в гл. [29]
Так как гибридизация орбиталей уже была описана в гл. [30]
Страницы: 1 2 3 4 5