Гигромицин
Cтраница 2
Интересный аналог 6-дезокси - К-гексозы - ее 5-кетопроизводное, вошедшее в литературу под названием б-дезокси-а - О-арабиногексофураноз - 5-улозы ( IX) - структурный компонент антибиотика гигромицина. Она была получена из антибиотика ангустмицина А; последний представляет собой нуклеозидоподобное вещество - N-гликозид аденина. [16]
Предельно допустимые - концентрации: стрептомицин 0 1 мг / м3 [51]; оксациллин 0 05 мг / м3, тетрациклин 0 1 мг / м3 [41], фл оримицин 0 1 мг / м3 [42], гигромицин Б 0 001 мг / м3 [43]; окситетрациклин 0 1 мг / м3, ампициллин 0 1 мг / м3, био. [17]
Строение гигромицина установлено почти полностью [ формула ( 39) ] i69 - i72 Молекула этого антибиотика содержит ароматический, ами-ноциклитный и гликозидный фрагменты. При гидролизе гигромицина ( 39) 6 N HC1 ( см. схему 4) образуется неоинозамин ( 42), полученный также при кислотном гидролизе близкого к гигромицину антибиотика № 1703 - 18 В ш ( см. стр. Поскольку эта реакция в ряду инозитов может сопровождаться обращением конфигурации, образование последнего означало, что продукт гидролиза гигромицина является либо неоинозамином ( 42), либо сциллоинозамином. Как видно из формулы ( 40), наличие метиленового мостика между гидроксилами у С и С4, С3 и С6, d и GS, С3 и Сs невозможно, так как эти гидроксилы транс-ориентированы. [18]
СБ-С6172; выбор между этими двумя положениями сделан не был. Продуктом жесткого щелочного гидролиза гигромицина ( кипячение с 10 % - ным NaOH в присутствии Zn в атмосфере N2) оказалась 3 4-диокси-а - метилкоричная кислота ( 41) 16Э, причем можно было предполагать, что в молекуле антибиотика она соединена амидной связью с остатком нео-инозамина. [19]
В табл. 2 приведены данные по кинетике десорбции гигромицина Б и окситетрациклина. При увеличении рН элюции окситетрациклина со смолы СБС-3 от 9.0 до 11 5 коэффициент диффузии увеличивается примерно в 10 раз, достигая значений 2.0 - 10 7, В случае десорбции гигромицина Б со смол КБ-4П-2 и СДВ-ЗТ имеет место аналогичная зависимость коэффициентов диффузии от рН элюирую-щего раствора. Коэффициенты диффузии увеличиваются на порядок, изменяясь от 2.0 - 10 - 8 до 2.9 - 10 - 7 см2 / сек. [20]
Многие из перечисленных антибиотиков являются давно известными н хорошо изученными соединениями, часто сравнительно простого строения. Лишь небольшое число представителей этой группы ( ксантоциллины, дрозофилин А, тетраоксистильбен, гигромицин, флавипин, квадри-линеатин, циклопальдовая и циклополовая кислоты, нидулин и дехлорнорнидулин) было открыто и химически исследовано за последние 5 - 7 лет; за это же время была обнаружена антибиотическая активность еще у нескольких ранее известных природных соединений ароматического ряда - метилового и этилового эфиров галловой кислоты и флоретина. Значительное внимание привлекли к себе за последние годы гладиоловая кислота и близкие к ней соединения, являющиеся производными фталевого альдегида; сходство строения и свойств позволяет объединить эти антибиотики в отдельную группу. [21]
Строение гигромицина установлено почти полностью [ формула ( 39) ] i69 - i72 Молекула этого антибиотика содержит ароматический, ами-ноциклитный и гликозидный фрагменты. При гидролизе гигромицина ( 39) 6 N HC1 ( см. схему 4) образуется неоинозамин ( 42), полученный также при кислотном гидролизе близкого к гигромицину антибиотика № 1703 - 18 В ш ( см. стр. Поскольку эта реакция в ряду инозитов может сопровождаться обращением конфигурации, образование последнего означало, что продукт гидролиза гигромицина является либо неоинозамином ( 42), либо сциллоинозамином. Как видно из формулы ( 40), наличие метиленового мостика между гидроксилами у С и С4, С3 и С6, d и GS, С3 и Сs невозможно, так как эти гидроксилы транс-ориентированы. [22]
Сравнивая медленную бесфакторную транслокацию с быстрой EF-G GTP-катализируемой транслокацией, важно отметить, что фактор, по-видимому, не снижает заметным образом тепловую энергию активации процесса; это наводит на мысль, что здесь катализ имеет преимущественно энтропийную природу. Ингибиторный анализ также показывает, что фактор не создает нового реакционного пути, идущего через промежуточные стадии в обход высокого активационного барьера, как это делает обычный энтальпийный катализатор: самые различные специфические ингибиторы транслокации ( БИОМИЦИН, спектиномицин, эритромицин, неомицин, канамицин, гентамицин, гигромицин В) действуют как на энзиматический, так и неэнзиматический процесс, указывая на существование одинакового транслокационного механизма, с одними и, теми же мишенями в обоих случаях. Следовательно, фактор элонгации катализирует процесс, скорее всего, путем создания лучших пространственных условий в рибосоме для того же самого, присущего рибосоме как таковой, транслокационного пути. Одним из способов сделать это могла бы быть простая фиксация одного из термически флуктуирующих под-состояний рибосомы, которое было бы благоприятно для транслокации. Такой фиксирующий или ориентирующий эффект присоединения EF-G как крупного дополнительного лиганда рибосомы кажется вероятным. [23]
Сопоставление полученных данных с электрохимическими свойствами антибиотиков позволяет объяснить указанный эффект. Аналогично происходит перезарядка ристомицина, который, обладая в кислых растворах двумя положительными зарядами, в щелочной области значений рН приобретает отрицательные заряды. Гигромицин Б, сорбированный так же как двухзарядный катион ( pKul - 7.1; рК 8.8), в щелочной области значений рН не ионизирован и, следовательно, не несет ни положительных, ни отрицательных зарядов. В результате происходящей перезарядки ионов в случае гигромицина Б исчезает электростатическое притяжение в системе сорбент-сорбат, а в случае антибиотиков окситетрациклина и ристомицина возникает электростатическое отталкивание между одноименно заряженными группами антибиотика сорбента. Это должно облегчать диффузию упомянутых веществ в трехмерной сетке ионитов. С уменьшением рН раствора, наоборот, происходит появление положительных зарядов в молекулах и эффект перезарядки сказывается в меньшей степени. При этом наряду с увеличением скорости диффузии происходит также и уменьшение активационных барьеров при движении ионов в фазе сорбента. [24]
Цистеин снимает действие гигромицина in vitro. [25]
Край пластинки погружают в растворитель не более чем на 0 5 см. После того как фронт растворителя поднимется примерно на 10 см, пластинку вынимают, отмечают линию фронта и оставляют на несколько минут на воздухе для испарения растворителя. Затем пластинку опрыскивают проявляющим реагентом. При наличии в пробе гигромицина на пластинке проявляется синее пятно на белом фоне, быстро буреющее на воздухе. Количественную оценку содержания препарата проводят визуально по интенсивности окраски и величине пятна пробы и стандартных растворов. [26]
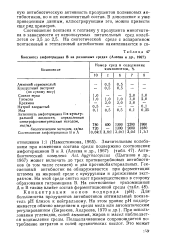 |
Биосинтез амфотерицииа В на различных средах ( Алеева и др., 1967. [27] |
Цыганов и др., 1967) может включать до трех противогрибковых антибиотиков ( в том числе гексаен) и два противобактериальных. Гек-саеновый антибиотик не обнаруживается при ферментации штамма на жировой среде с кукурузным и дрожжевым экстрактом. На этой среде синтез идет преимущественно в сторону образования гигромицина В. Для-большинства продуцентов антибиотиков оптимальный показатель рН близок к нейтральному. При использовании углеводов, солей аммония, жиров и масел наблюдается подкисление среды. Подщелачиванием сопровождается потребление нитратов и солей органических кислот. [28]
Строение гигромицина установлено почти полностью [ формула ( 39) ] i69 - i72 Молекула этого антибиотика содержит ароматический, ами-ноциклитный и гликозидный фрагменты. При гидролизе гигромицина ( 39) 6 N HC1 ( см. схему 4) образуется неоинозамин ( 42), полученный также при кислотном гидролизе близкого к гигромицину антибиотика № 1703 - 18 В ш ( см. стр. Поскольку эта реакция в ряду инозитов может сопровождаться обращением конфигурации, образование последнего означало, что продукт гидролиза гигромицина является либо неоинозамином ( 42), либо сциллоинозамином. Как видно из формулы ( 40), наличие метиленового мостика между гидроксилами у С и С4, С3 и С6, d и GS, С3 и Сs невозможно, так как эти гидроксилы транс-ориентированы. [29]
 |
Тестирование промоторных конструкций в трансгенных растениях. [30] |
Страницы: 1 2 3