Гидрат - серная кислота
Cтраница 1
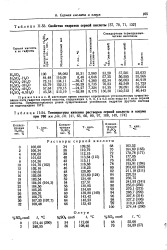
Гидраты серной кислоты имеют определенные температуры кристаллизации ( ркс. [1]
Если гидраты серной кислоты и пиросерную кислоту большинство исследователей склонны принимать за комплексы, то, естественно, следует и серную кислоту считать за комплексное соединение; у ней, может быть, лишь в меньшей степени, чем у всех остальных соединений, сохраняются характерные свойства комплексных веществ. Однако многочисленные литературные данные вполне четко подтверждают комплексный характер и серной кислоты, который почему-то совершенно не принимался во внимание всеми теми химиками-органиками, которые занимались и занимаются изучением реакций сульфирования. [2]
При этом образуются гидраты серной кислоты. [3]
Таким образом, имеются все основания считать гидрат серной кислоты солью. [4]
 |
Свойства гидратов серной кислоты. [5] |
В настоящее время считают определенно установленным существование пяти гидратов серной кислоты, содержащих 1, 2, 3, 4 и 6 5 моль воды на 1 моль серной кислоты. [6]
В настоящее время считают определенно установленным существование пяти гидратов серной кислоты, содержащих 1, 2, 3, 4 и 6 5 моль воды на 1 моли серной кислоты. [7]
Можно предположить, что действительно при растворении серной кислоты в воде образуются соединения - гидраты серной кислоты. Чтобы их обнаружить и определить состав, следует рассмотреть зависимость температур замерзания растворов серной кислоты от их концентрации. [8]
В целом его гидратяая теория состоит в том, что во время процесса нитрации происходят два параллельных явления а именно: I) нитрация клетчатки моногидратом азотной кислоты и 2) разрушение клетчатки гидратом серной кислоты. [9]
При образовании моногидрата азотной кислоты выделяется всего 1300 кал / моль, поэтому можно считать, что основное количество воды, содержащейся в нитрующей смеси и образующейся в процессе нитрации, связывается в виде гидратов серной кислоты, и тем самым равновесие при нитрации сдвигается в сто-рону образования эфира целлюлозы. [10]
 |
Диаграмма кипения водных растворов азотной кислоты под атмосферным давлением. [11] |
Для получения концентрированной азотной кислоты ( более 68 %) обычно перегоняют разбавленную азотную кислоту в присутствии крепкой серной кислоты как водоотнимающего средства. Крепкая серная кислота связывает воду, содержащуюся в разбавленной азотной кислоте, образуя гидраты серной кислоты, кипящие при температуре более высокой, чем 100 % - ная НМОз. [12]
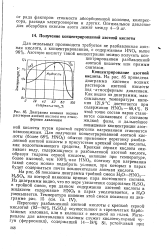 |
Диаграмма кипения водных растворов азотной кислоты под атмосферным давлением. [13] |
Для получения концентрированной азотной кислоты ( более 68 % HNOs) обычно применяют перегонку разбавленной азотной кислоты в присутствии крепкой серной кислоты, как водоотнимающего средства. Крепкая серная кислота свя-зываег воду, содержащуюся в разбавленной азотной кислоте, образуя гидраты серной кислоты, кипящие при температуре, более высокой, чем 100 % - ная HNO3, поэтому при нагревании такой смеси можно подобрать условия, при которых в парах будет содержаться почти исключительно азотная кислота. [14]
Общеизвестно, что в первом же своем калориметрическом исследовании, а именно в работе, опубликованной в 1839 г. в Анналах Либиха [1], Гесс измерил теплоты разбавления серной кислоты п, сопоставляя состав смеси с количествами выделенного тепла, обнаружил этим путем существование нескольких гидратов серной кислоты. [15]
Страницы: 1 2