Гидрат - нитрат
Cтраница 1
Гидраты нитрата Ре ( Ш) получают взаимод. [1]
 |
Установка для получения безводных нитратов. [2] |
Гидраты нитратов состава Ьп ( МО3) з-гс Н2О имеются в продаже, но они непригодны для получения безводных нитратов. [3]
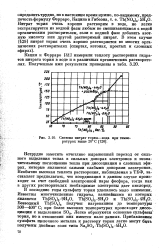 |
Система нитрат тория-вода при температурах выше 20Ъ С. [4] |
Кацин и Ферраро [41] измерили теплоту растворения гидратов нитрата тория в воде и в различных органических растворителях. [5]
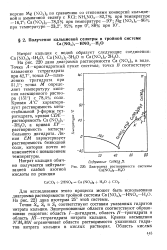 |
Диаграмма растворимости системы Са ( М03 2 - Н2О. [6] |
Точки Sz, Ss и S4 соответствуют составам указанных гидратов нитрата кальция. Заштрихованные области соответствуют образованию гидратов: область / - дигидрата, область / / - тригидрата и область / / / - тетрагидрата нитрата кальция. Кривая насыщения N M MN ограничивает области растворимости указанных гидратов нитрата кальция в кислых растворах. [7]
Точки S2, Ss и S4 соответствуют составам указанных гидратов нитрата кальция. Заштрихованные области соответствуют образованию гидратов: область / - дигидрата, область / / - тригидрата и область / / / - тетрагидрата нитрата кальция. Кривая насыщения N M - MN ограничивает области растворимости указанных гидратов нитрата кальция в кислых растворах. [8]
Однако, несмотря на то что при добавлении макроколичеств второго компонента температура плавления гидрата нитрата кальция понижается, коэффициент распределения Mg ( NO3) 2 - 6H2O в Ca ( N03) 2 - 4H2O при содержании соли магния 3 - 10 - 3 - 3 - 10 - 4 % ( масс.) оказывается больше единицы. [9]
Полученный раствор упаривают при 80 - 85 С до начала кристаллизации ( гексагпдрат выделяется при температуре ниже 89 9 С) и дают остыть. При этом выпадает шсстиводнын гидрат нитрата магния в виде бесцветных кристаллов. [10]
Ранее уже были рассмотрены структуры нескольких гидратов оксосолей кальция. Это хорошо иллюстрируют структуры трех гидратов нитрата кальция. Дигндрат имеет слоистую структуру. Во всех трех структурах водородная связь осуществляется только между соседними структурными единицами: слоями, тетрамерами или димерами. [11]
По-видимому, под действием безводного хлористого водорода и ионов металла азотная кислота разлагается на ангидрид и воду, которая образует гидраты нитратов и удаляется из сферы реакции при осаждении последних. Использование в качестве реакционной среды расплавленной соли еще не изучено в достаточной степени. Основные трудности таких методов синтеза связаны с выделением продукта и с применением высоких температур. Этот метод заслуживает дальнейшего изучения. [12]
Однако, судя по кривым ТГ, приводимым в том же исследовании, уже к 300 - 350 С основная масса воды из кристаллогидрата удалена. Исходя из этого, а также из наличия на термических кривых довольно протяженного плато, характеризующегося Г - const и предшествующего последним эндоэффектам, можно предположить, что при термолизе гидратов нитратов Ln и Ага к 300 С мы имеем дело уже с практически безводной солью. [13]
Нагревание при обезвоживании производят со скоростью 3 град / мин от комнатной температуры примерно до 600 С. Определяют, какое вещество получается в результате такой термической обработки, образованию каких соединений соответствуют отдельные ступени на кривой зависимости массы вещества от температуры, каков состав выделенных из водного раствора гидратов нитрата тория. [14]
Термическое разложение гидратов нитратов кобальта, цинка, меди и хрома. [15]
Страницы: 1 2