Гидрат - окись
Cтраница 3
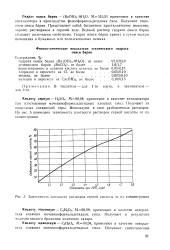 |
Зависимость плотности растворов серной кислоты от их концентрации. [31] |
Гидрат окиси бария - ( ВаОН) 2 - 8Н2О, М 315 51 применяют в качестве катализатора в производстве фенолформальдегидных смол. Получают гашением окиси бария. Представляет собой бесцветное кристаллическое вещество, хорошо растворимое в горячей воде. Водный раствор гидрата окиси бария обладает щелочными свойствами. [32]
Гидрат окиси бария упаковывают в мешки из полиэтиленовой пленки, вложенные в четырехслойные бумажные мешки или льно-джуто-кенафные мешки; нетто их не более 50 кг. [33]
Гидрат окиси бария, поставляемый на экспорт, упаковывают в мешки из полиэтиленовой пленки, вложенные в пятислойные бумажные битуми-ровашше мешки или в льно-джуто-кенафные мешки, нетто которых не более 50 кг. [34]
Гидраты окиси тетраалкиламмония - сильные основания, полностью диссоциированные на ионы. [35]
 |
Спектры поглощения растворов Hg ( II ( Ю мг / л в 6 М НС1 ( 1, 4 М NaBr ( 2 и 4 М NaJ ( 3 ( толщина слоя 1 см. [36] |
Гидрат окиси ртути очень неустойчив, и равновесие Hg ( OH) 2 i HgO H20 сильно смещено вправо. [37]
Гидрат окиси цетила ( этал) С32Н330 - f - НО не изменяется на воздухе, согласно общему правилу, что чем сложнее тело, тем оно труднее окисляется выше. [38]
Гидрат окиси амила с Мп02 и S03 дает, по Балару, валерианокислую окись амила. [39]
Гидрат окиси амила при повторенных перегонках с азотной кислотой дает, по Дюма и Штассу, соединение VaO - j - НО. По Балару, азотная кислота не действует в холоде, а при разгорячении происходит сильная реакция и образование валериановой кислоты, синильной и азотистокислой окиси амила. Пары гидрата окиси амила при пропускании чрез нагретую смесь кали с известью дают валерианокислое кали. [40]
Гидрат окиси цетила - этал Cs2H330 - j - НО с кали и известью, отделяя водород, переходит в эталовую кислоту С32Н3103 - ( - НО. Азотная кислота разлагает его при окислении, образуя пимелиновую, адипи-новую и янтарную кислоты. [41]
Гидраты окисей днфснплнолоннсв являются сильными основаниями, сравнимыми с четвертичными аммониевыми п сульфониевыми основаниями. [42]
Гидрат окиси бария - белые, слегка окрашенные кристаллы. Легко поглощает углекислый газ из воздуха. Растворим в воде, имеет щелочную реакцию. Находит применение в ряде синтезов лекарственных препаратов. [43]
Гидрат окиси бария, гидроокись бария, или едкий барит, Ва ( ОН) 2 - 8Н2О, прозрачные моноклинич. Водный раствор является сильной щелочью, жадно поглощающей СО2 из воздуха. Применение довольно ограничено и в технике широкого значения не имеет. В Германии производство его достигает около 700 т в год. Кроме того применяется для нейтрализации смол, масел, воска и для обессахаривания патоки. [44]
Гидраты окиси тетраалкиламмония - сильные основания, полностью диссоциированные на ионы. [45]
Страницы: 1 2 3 4