Гидрат - окись - кальций
Cтраница 3
Растворы гидрата окиси кальция и гидрата окиси магния можно легко получить, если полученные при сжигании кальция и магния в кислороде окислы этих металлов взболтать с водой. Растворы этих гидратов окислов обладают характерными особенностями: они окрашивают красную лакмусовую бумагу в синий цвет; они мылки наощупь. [31]
Выщелачивание гидрата окиси кальция из бетона сопровождается снижением его концентрации. [32]
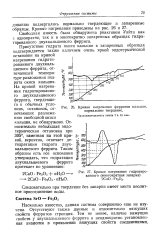 |
Кривая нагревания гидратиро. [33] |
Присутствие гидрата окиси кальция в запаренных образцах подтверждается также наличием очень яркой эндотермической остановки на кривой нагревания гидрати-рованного двухкальциевого феррита, отвечающей температуре разложения гидрата окиси кальция. [34]
Кристаллы гидрата окиси кальция, пронизывая гелеобразные, рыхлые новообразования гидрата двухкальциевого силиката, как бы армируют его, тем самым увеличивая прочность. [35]
Растворение гидрата окиси кальция значительно ускоряется, если в воде содержится некоторое количество свободной минеральной или органической кислоты. При этом кроме физического растворения ( выщелачивания) наблюдается и химическое растворение. [36]
Растворимость гидрата окиси кальция ( в пересчете на СаО) в воде небольшая: при 0 - 0 13, 20 - 0 12, 50 - 0 10 г / 100 г воды. [37]
Отложение гидратов окисей кальция и магния в асбестовых диафрагмах и изменение протекаемости последних при этом было рассмотрено выше. [38]
Связывание гидрата окиси кальция значительно интенсифицируется при тепловой обработке бетона, что приводит к существенному снижению величины рН поровой жидкости. [39]
Абсолютно сухие гидрат окиси кальция и хлор не вступают в реакцию; хлор только адсорбируется известью. В производственных условиях хлорированию подвергают пушонку, содержащую менее 1 % свободной влаги; применяющийся для этой цели разбавленный воздухом хлор также содержит небольшое количество влаги. Даже небольшая влажность исходных веществ обеспечивает начало реакции гидролиза хлора с нейтрализацией образующихся кислот известью. Затем гидролиз продолжается за счет воды, выделяющейся при хлорировании из гидрата окиси кальция, и все новые количества извести вступают в процесс; образуется ряд соединений, из которых и состоит хлорная известь ( стр. [40]
Так как гидрат окиси кальция выделяется в осадок, то водный раствор NaOCl, полученный из гипохлорита кальция менее загрязнен побочными солями, чем NaOCl, полученный из хлора и щелочи. [41]
Кремнезем и гидрат окиси кальция во влажной среде способны реагировать при обычной температуре; поэтому и при смешении динасовой массы с известковым молоком окись кальция в какой-то степени должна связываться с кремнеземом в гидросиликаты кальция. Количественно реакция определяется зерновым составом массы, количеством введенной окиси кальция и условиями смешения. [42]
При хранении гидрат окиси кальция превращается под воздействием углекислого газа и воды в углекислый кальций, а соли кислот разрушаются до свободных кислот. Аналогичный процесс проходит и на растениях. Поэтому для предотвращения ожогов растений при применении арсената кальция необходимо к препарату добавить двойное количество свежегашеной извести-пушенки. [43]
Абсолютно сухие гидрат окиси кальция и хлор не вступают в реакцию; хлор только адсорбируется известью. [44]
Шлам, содержащий гидрат окиси кальция, должен перед сбросом отстаиваться в больших ямах. [45]
Страницы: 1 2 3 4