Гидрат - окись - галлий
Cтраница 1
Гидрат окиси галлия Оа2Эз НаО обладает амфотерными свойствами, причем кислотный характер доминирует. [1]
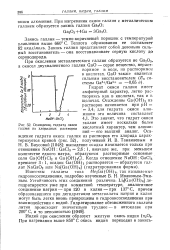 |
Осаждение гидрата окиси галлия из хларидных растворов. [2] |
Гидрат окиси галлия имеет амфотерный характер, легко растворяясь как в кислотах, так и в щелочах. Это значит, что гидрат окиси галлия имеет несколько более кислотный характер, чем алюминий - его высший аналог. [3]
Гидрат окиси галлия Ga ( OH) 3, как и А1 ( ОН) 3, проявляет амфотерные свойства. [4]
Гидрат окиси галлия Ga ( OH) 3, осажденный совместно с А1 ( ОН) 3 при выкручивании или карбонизации и превращенный прокаливанием в Ga2O3) с глиноземом поступает на электролиз и выделяется на катоде вместе с алюминием. В этом случае галлий не только пропадает для народного хозяйства, но и загрязняет алюминий. [5]
Малая растворимость гидратов окисей галлия и индия ( произведение растворимости равны соответственно 10 - 33 и 10 - 33) и относительно малая величина рН начала осаждения позволяют предположить, что механизм соосаждения галлия и индия, по-видимому, заключается в механическом захвате осадком фосфата кальция золей гидроокисей галлия и индия. Поскольку гидроокись галлия амфотерна и заметно растворима в аммиаке, мы наблюдаем падение процента соосаждения галлия с повышением значения рН раствора; этого явления не наблюдается для индия. [6]
Гидратированный фторид GaF3 - 3 - 3 5Н20 образуется при растворении окиси или гидрата окиси галлия во фтористоводородной кислоте. Безводная соль представляет собой белое твердое вещество; она начинает возгоняться при 800, а при 950 упругость пара этой соли достигает 1 атм. Она слабо растворима как в холодной, так и в теплой воде. Трифторид галлия находится в таком же отношении ктри-хлориду, как трифторид алюминия к своему трихлориду. Это сходство с алюминием относится также к образованию комплексов. [7]
С, и при 950 С упругость пара достигает 760 мм рт. ст. Получить GaF3 можно различными способами - действием фтора на металлический галлий, окись галлия, сульфид галлия или при растворении гидрата окиси галлия в плавиковой кислоте. В последнем случае фторид выделяется в виде кристаллогидрата с тремя молекулами воды. [8]
Образование белого осадка при пропускании H2S в сильнокислый раствор соли галлия, наблюдавшееся Лекоком де Буабодрапом в 1881 г., относительно которого было предположено, что происходит образование сульфида, объясняется ( Brukl), по-видимому, тем, что при этом вследствие гидролиза возникает гидрат окиси галлия; действительно, так как сульфид галлия в соприкосновении с водой неустойчив, его нельзя получить пз водных растворов. [9]
Образование белого осадка при пропускании H2S в сильнокислый раствор соли галлия, наблюдавшееся Лекоком де Буабодроном в 1881 г., относительно которого было предположено, что происходит образование сульфида, объясняется ( Brukl), по-видимому, тем, что при этом вследствие гидролиза возникает гидрат окиси галлия; действительно, так как сульфид галлия в соприкосновении с водой неустойчив, его нельзя получить из водных растворов. [10]
Образование белого осадка при пропускании H2S в сильнокислый раствор соли галлия, наблюдавшееся Лекоком де Вуабодроном в 1881 г., относительно которого было предположено, что происходит образование сульфида, объясняется ( Brukl), по-видимому, тем, что при этом вследствие гидролиза возникает гидрат окиси галлия; действительно, так как сульфид галлия в соприкосновении с водой неустойчив, его нельзя получить из водных растворов. [11]
На воздухе галлий устойчив, воду не разлагает, но растворяется в кислотах и щелочах. Гидрат окиси галлия Ga ( OH) s амфотерен. Добавка галлия к магниевым сплавам увеличивает их прочность и ковкость. [12]
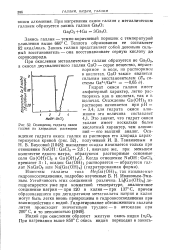 |
Осаждение гидрата окиси галлия из хларидных растворов. [13] |
Гидрат окиси галлия имеет амфотерный характер, легко растворяясь как в кислотах, так и в щелочах. Это значит, что гидрат окиси галлия имеет несколько более кислотный характер, чем алюминий - его высший аналог. [14]
После опубликования Заметки Менделеева ( ст. 11) в очередном выпуск Отчетов Парижской академии наук от 6 декабря 1875 г. появилось новое-сообщение Лекок де - Буабодрана О некоторых свойствах галлия ( С. Здесь указывается, что если прибавить уксусной кислоты к аммиачному раствору сульфатов или хлоридов галлия и Zn, то почти весь галлий отделяется в форме белого осадка желатинообразных хлопьев. Таким образом, оказалось, что гидрат окиси галлия имеет аморфный характер, как это и предвидел Менделеев. [15]
Страницы: 1 2