Гидрат - пятиокись
Cтраница 1
Гидраты пятиокисей всех элементов в той или иной мере растворимы в сильных кислотах и растворах щелочей. Однако V2O5, Nb2O5 и Та2О5 правильнее считать окислами кислотными, так как они образуют соли преимущественно с окислами основного характера. Способность соединений пятивалентных элементов подгруппы гидролизоваться уменьшается в направлении от ванадия к танталу. [1]
 |
Некоторые свойства элементов подгруппы ванадия. [2] |
Гидраты пятиокисей всех трех элементов в той или иной мере растворимы в сильных кислотах и растворах щелочей. Однако окислы V2Os, РЛ Об и Ta2Os правильнее считать окислами кислотными, так как они образуют соли преимущественно с окислами основного характера. [3]
Сурьмяная Гидрат пятиокиси висмута, кислота висмутовая кислота. [4]
При дальнейшем действии воды гидролиз идет с образованием гидрата пятиокиси ниобия. [5]
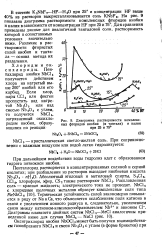 |
Диаграмма растворимости комплексных фторидов ниобия ( и тантала и калия при 25 и 75. [6] |
При дальнейшем воздействии воды гидролиз идет с образованием гидрата пятиокиси ниобия. [7]
Первая ветвь изотермы на диаграмме растворимости отвечает растворимости гидрата пятиокиси ниобия во фтористоводородной кислоте. Из очень концентрированных ( по HF) растворов выделяется NbF5, причем растворимость пентафторида ниобия осложняется явлением пересыщения растворов. [8]
Поскольку все-таки природа этого соединения еще неизвестна, то его лучше называть гидратом пятиокиси сурьмы. Это белый порошок, растворимый как в соляной кислоте, так и в растворе КОН. В воде он практически не растворяется, однако в значительной мере переходит в коллоидный раствор, если обрабатывать свежеосажденный препарат водой. [9]
Поскольку все-таки природа этого соединения еще неизвестна, то его лучше называть гидратом пятиокиси сурьмы. Это белый порошок, растворимый как в соляной кислоте, так и в растворе КОН. В воде он практически не растворяется, но, однако, в значительной мере переходит в коллоидный раствор, если обрабатывать свежеосажденный препарат водой. [10]
При гидролизе кислых растворов SbCl5 в интервале температур от 0 до 100 или при нагревании растворов соединения К3 [ ЗЬС16 ] с азотной кислотой образуются гидраты пятиокиси сурьмы Sb205 - тгН20 ( п 1, 2, 3, 4, 5 и 6) в виде белых осадков. [11]
Гидрат можно легко получить или путем растворения металлической сурьмы в азотной кислоте с последующим выпарпвапием кпсло-ты, или гидролизом пентахлорпда сурьмы. Прокалипанпе гидрата пятиокиси сурьмы следует проводить при температуре около 270 С. Выше этой температуры происходит постепенное отщепление кислорода, и продукт загрязняется четырехокпсью сурьмы. При прокаливании ниже 270 С процесс дегидратации может не доптп до конца. [12]
Мышьяковая и сурьмяная кислоты в виде соединений с указанным выше составом известны только в растворах или в виде солей ( см. стр. Является ли гидрат пятиокиси висмута соединением с определенным составом [ висмутовой кислотой ВЮг ( ОН) или ВЮ ( ОН) з ], точно не установлено, однако известны соли с вполне определенным составом - производные висмутовой кислоты ( см. стр. [13]
Поскольку все-таки природа этого соединения еще неизвестна, то его лучше называть гидратом пятиокиси сурьмы. Это белый порошок, растворимый как в соляной кислоте, так и в растворе КОН. В воде он практически не растворяется, но, однако, в значительной мере переходит в коллоидный раствор, если обрабатывать свежеосажденный препарат водой. [14]
Пятиокись сурьмы Sb2Os образуется обезвоживанием гидратированной пятиокиси сурьмы. Гидрат можно легко получить или растворением металлической сурьмы в азотной кислоте с последующим выпариванием кислоты, или гидролизом пентахлорида сурьмы. Прокаливают гидрат пятиокиси сурьмы при 270 С. Выше этой температуры происходит постепенное отщепление кислорода и продукт загрязняется четырехокисью сурьмы. При прокаливании ниже 270 С процесс дегидратации может не дойти до конца. Все окислы сурьмы светло-желтого цвета, при комнатной температуре на воздухе устойчивы. [15]
Страницы: 1 2