Гидрат - трехокись
Cтраница 1
Гидрат трехокиси - р енистая кислотаН 2ReO4 получается в виде черного аморфного порошка ( пл. При нагревании выше 100 начинает обезвоживаться. Не растворима в воде, мало растворима в соляной, серной и фосфорной кислотах. Легко растворяется в горячих растворах щелочей, хорошо в азотной кислоте и перекиси водорода, окисляющих ее до рениевой кислоты. [1]
Гидрат трехокиси мышьяка - мышьяковистого ангидрида - слабая трехосновная ( в отличие от фосфористой) кислота; гидрат трехокиси сурьмы амфотерен, гидрат трехокиси висмута - слабое, практически не растворимое в воде основание. [2]
Гидрат трехокиси мышьяка - мышьяковистого ангидрида - слабая трехосновная ( в отличие от фосфористой) кислота; гидрат трехокиси сурьмы амфотерен, гидрат трехокиси висмута - слабое, практически нерастворимое в воде основание. [3]
Какой химический характер имеет гидрат трехокиси молибдена. [4]
При упаривании бесцветного водного раствора MoOF4 выпадают гидраты трехокиси молибдена. [5]
Гидрат закиси-окиси урана легко окисляется на воздухе до гидратов трехокиси, растворяется в кислотах с образованием смеси солей четырех - и шестивалентного урана. [6]
Гидрат трехокиси мышьяка - мышьяковистого ангидрида - слабая трехосновная ( в отличие от фосфористой) кислота; гидрат трехокиси сурьмы амфотерен, гидрат трехокиси висмута - слабое, практически не растворимое в воде основание. [7]
Гидрат трехокиси мышьяка - мышьяковистого ангидрида - слабая трехосновная ( в отличие от фосфористой) кислота; гидрат трехокиси сурьмы амфотерен, гидрат трехокиси висмута - слабое, практически нерастворимое в воде основание. [8]
Разнообразие соединений со структурами, включающими ураниловую связь, как следует из изложенного выше, обусловлено амфотерным характером гидрата трехокиси урана с достаточно четко выраженными как основными, так и кислотными свойствами. Поскольку основные свойства выражены больше, чем кислотные, реакционная способность трехокиси по отношению к кислотам со сколь-угодно слабыми свойствами проявляется больше, чем по отношению к слабым основаниям. Трехокись урана не реагирует с окисью бериллия, образующей амфотерную гидроокись, и с окисью алюминия, гидрат которой вступает в реакцию только с сильными кислотами. [9]
Гидрат трехокиси мышьяка - мышьяковистого ангидрида - слабая трехосновная ( в отличие от фосфористой) кислота; гидрат трехокиси сурьмы амфотерен, гидрат трехокиси висмута - слабое, практически нерастворимое в воде основание. [10]
Гидрат трехокиси мышьяка - мышьяковистого ангидрида - слабая трехосновная ( в отличие от фосфористой) кислота; гидрат трехокиси сурьмы амфотерен, гидрат трехокиси висмута - слабое, практически не растворимое в воде основание. [11]
Известен ряд гидратов UOs: UOs - O ( илиШиО, UOs - 2HaO ( или НШОо), 2UOs - H2O ( или HzUzOi) и др. Гидраты трехокиси урана гораздо более устойчивы, чем гидраты двуокиси. Гидраты UOs плохо растворимы в воде. [12]
Гидраты трехокиси урана гораздо более устойчивы, чем гидраты двуокиси. Гидраты UOs плохо растворимы в воде. [13]
Значения w определяют опытным путем для каждого из перерабатываемых веществ. При сушке гранулированного гидрата трехокиси и гидрофторировании двуокиси урана w 2500 кг / ( м2 - ч); при восстановлении трехокиси урана до двуокиси ш 3150 кг / ( м2 - ч); при соблюдении этих ограничений режим работы печи наиболее стабилен. [14]
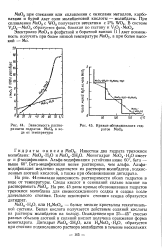 |
Зависимость растворимости гидратов МоО3 в воде от температуры.| Кривые обезвоживания гидратов МоО3. [15] |
Страницы: 1 2