Гидрат - хлорид
Cтраница 2
ОРТА получают термическим разложением гидратов смешанных хлоридов. С ростом температуры хлор удаляется и степень кристалличности возрастает. При 800 С хлор удаляется полностью, и система распадается на отдельные оксиды. [16]
Таким образом, изомерия гидратов хлорида хрома ( III) обусловлена различным распределением одних и тех же групп ( НаО и С1 -) между внутренней и внешней координационными сферами и может служить примером гидратной изомерии ( разд. [17]
Это соединение получают кристаллизацией гидрата хлорида никеля из пиридина. Таким же способом получают аналогичное соединение железа, растворимое в органических растворителях. [18]
Чтобы установить, какой металл образует данный гидрат хлорида, рассчитаем атомную массу металла в предположении нескольких возможных степеней его окисления. [19]
В растворах устанавливается равновесие между тремя гидратами хлорида хрома, соответственно между их ионами, причем состояние равновесия зависит как от температуры, так и концентрации и состава изомеров. На холоду и в разбавленных растворах в основном присутствует сине-фиолетовый хлорид; в очень концентрированных растворах - зеленый. При нагревании равновесие сдвигается в сторону образования темно-зеленого хлорида хрома. Посмотрим теперь как протекают эти реакции на опыте. [20]
Процесс обезвоживания осложняется следующим: во-первых, гидраты хлорида магния плавятся в своей кристаллизационной воде при относительно невысоких температурах, вследствие чего частично обезвоженный продукт оплавляется, тем самым затрудняя дальнейшее обезвоживание; во-вторых, после удаления из гек-сагидрата четырех молекул воды начинается заметный гидролиз. [21]
Свежеприготовленный раствор, содержащий 2 665 г гидрата хлорида хрома ( III) состава СгС1зНх20б при действии избытка раствора нитрата серебра сразу образует 2 87 г осадка. [22]
Далее от этой точки идет третья ветвь кристаллизации следующего гидрата хлорида стронция. Химический анализ показал, что в соли содержится 36.21 % хлор-иона или 80.97 % хлористого стронция, что близко отвечает шестиводному гидрату. Полученная изотерма растворимости исследуемой системы аналогична диаграмме, установленной предыдущими исследователями. [23]
При работе по гидридному методу в качестве восстановителя широко используют гидрат хлорида олова ( II), тетрагидроборат натрия и цинковый порошок. Известен также способ получения гидрида путем электрохимического восстановления. [24]
При сравнении отдельных ветвей кристаллизации одноводного хлорида лития с ветвями выделения гидратов хлорида стронция наблюдается относительно высокий эффект высаливания из раствора последних солью хлористого лития, как это имело место в присутствии хлорида натрия. [25]
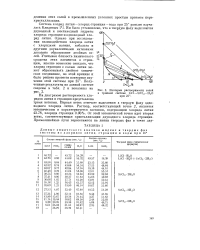 |
Изотерма растворимости солей. [26] |
Им было установлено, что в твердую фазу выделяются двуводный и шестиводный гидраты хлорида стронция и одноводный хлорид лития. Однако при исследовании взаимодействия хлорида лития с хлоридами магния, кобальта и другими двувалентными катионами доказано образование двойных солей. [27]
Существует несколько способов подавления гидролиза ( стадия 4), протекающего при нагревании гидратов хлоридов металлов. Наиболее простым из них является добавление к нагреваемому кристаллогидрату, например к MgCl2 - 6H2O, вещества, выделяющего НС1 при термолизе. Чаще всего с этой целью используют хлорид аммония. [28]
Безводный СиС12 получают хлорированием меди значительным избытком хлора, действием сухого хлористого водорода на порошок CuSO4 или CuSO4 - H2O, обезвоживанием гидратов хлорида меди. Так, СиС12 - 2Н2О теряет воду при нагревании до 100 С или при 150 С в потоке хлористого водорода. [29]
Страницы: 1 2 3