Гидратация - молекула
Cтраница 2
В первом приближении также можно находить и энергию гидратации молекул, суммируя энергии гидратации отдельных гидрофильных групп или участков структуры молекулы. [16]
В то же время иногда разница в энергиях гидратации молекул маскируется разницей в энергиях чистых жидкостей, как, например, в случае пары BuNH2 - i - BuNH2, для которых & H S практически равны, но ДЯ /, на 1 9 кДж моль - более экзотер-мична для нормального бутиламина. [17]
Наиболее сложно влияет на образование мицелл неионогенных ПАВ изменение гидратации молекул при их ассоциации. Существенную роль в гидратации мицелл неионогенных ПАВ играет образование оксониевых соединений воды с полиоксиэтиленовыми группами молекул и водородных связей. В ряде работ [ 135 - 139 было показано, что максимальное число гидратации оксиэтилено-вых групп равно четырем. [18]
Раствор кислоты находится в межпузырьковом пространстве и удерживается там вследствие гидратации молекул ПАВ. При контакте с карбонатной породой в призабонтюй зоне пласта ненокислота нейтрализуется не сразу, а лишь частично, что особенно важно при обработке высокотемпературных скважин. Этим удается постепенно закачать ненокислоту с достаточной активностью в более удаленные зоны пласта. [19]
В настоящее время амфотерность рассматривается на основе процессов комплексообразования и гидратации молекул гидре-ксидов и образующихся из них ионов. В работе сделана попытка уточнить и конкретизировать эти представления на основе стереохимии элементов, имеющих атомы с вакантными уэ-орбиталями с низким уровнем энергии в молекулах. [20]
В настоящее время амфотерность рассматривается на основе процессов комплексообразования и гидратации молекул гидроксидов и образующихся из них ионов. В работе сделана попытка уточнить и конкретизировать эти представления на основе стереохимии элементов, имеющих атомы с вакантными р-орбиталями с низким уровнем энергии в молекулах. [21]
Нередко проявляется поляризующее действие молекул воды на молекулы соли: гидратация молекул соли сопровождается усилением полярности связи в ней. [22]
Внутримолекулярные водородные связи в двухзамещенных производных бензола приводят к уменьшению гидратации молекул. Вследствие этого разность - ДОд - AG увеличивается и абсолютное значение - ДС возрастает. [23]
Внутримолекулярные водородные связи в двухзамещенных производных бензола приводят к уменьшению гидратации молекул. [24]
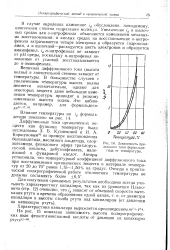 |
Зависимость предельного тока формальдегида от температуры. [25] |
В случае акролеина изменение id обусловлено, невидимому, изменением степени гидратации молекул. Увеличение id в щелочных средах для о-нитрофенола объясняется изменением механизма восстановления: в кислых средах на восстановление о-нитрофенола затрачивается четыре электрона и образуется гидроксил-амин, а в щелочной-расходуется шесть электронов и образуется аминофенол. [26]
Ассоциация молекул многих высокомолекулярных веществ с образованием более крупных агрегатов, а также гидратация молекул ряда соединений и, наконец, растворение многих веществ в воде несомненно связаны с возникновением водородных мостиков или связей. [27]
Допуская даже приближенность этих расчетов, следует сказать, что гидратация ионов все же больше гидратации молекул, и игнорировать этот фактор при рассмотрении теории устойчивости нельзя. При современном состоянии наших знаний правильнее сказать, что устойчивость лиофобных золей обусловлена гидратацией ионов стабилизатора, и всякое понижение диссоциации ( сжатие диффузного слоя) должно повлечь за собой уменьшение гидратации и, следовательно, устойчивости. В настоящее время наши знания в области С-потенциала дают возможность построить теорию устойчивости, беря в основу именно эту величину, связанную с гидратацией. Такая схема не может встретить возражений, пока мы имеем дело с заряженными частицами. Однако существуют коллоидные системы, частицы которых не несут заряда и все же остаются стабильными. [28]
Допуская даже приближенность этих расчетов, следует сказать, что гидратация ионов все же больше гидратации молекул, и игнорировать этот фактор при рассмотрении теории устойчивости нельзя. [29]
ЭМП могут поляризовать боковые цепи белковой молекулы, вызывая разрывы водородных связей и изменяя зону гидратации молекул. Существует предположение, что сильные ПМП могут влиять на ориентацию макромолекул, в частности РНК и ДНК, и тем самым изменять биологические процессы. [30]
Страницы: 1 2 3 4