Гидратация - соединение
Cтраница 2
Сопоставление вычисленных по формуле Борна теплот гидратации соединений NaF, NaCl, KF и КС1 с их опытными значениями ( см. табл. 2.1) показывает, что теоретические величины завышены по сравнению с опытными, хотя качественно формула Борна правильно передает взаимную связь между энергиями ( теплотами) сольватации и свойствами ионов. [16]
Сопоставление вычисленных по формуле Борна теплот гидратации соединений NaF, NaCl, KF и К. Борна правильно передает взаимную связь между анергиями ( теплотами) сольватации и свойствами ионов. [17]
Сопоставление вычисленных по формуле Борна теплот гидратации соединений NaF, NaCl, KF и КС1 с их опытными значениями ( см. табл. 12) показывает, что теоретические величины завышены, хотя качественно формула Борна правильно передает взаимную связь между энергиями ( теплотами) сольватации и свойствами ионов. [18]
Очевидно, особенности кристаллических структур и энергии гидратации соединений и ионов играют важную роль при определении устойчивости трехвалентного состояния. Таким образом, характерное положительное трехвалентное состояние лантанидов не находится в прямой связи с числом валентных электронов внешней 4 / - подоболочки, а является отчасти случайным результатом почти постоянной небольшой разности крупных неличин энергий ( с одной стороны, ионизационных по тенциалов и с другой - энергий гидратации и энергий образования кристаллов), наблюдаемой во всем интер нале четырнадцати атомных номеров. Поэтому, если бы мы имели более расширенную периодическую систему элементов, содержащую большое число / переходных рядов, то могли ожидать, что 5 / - элементы были бы более характерными представителями таких / - рядов. [19]
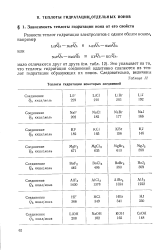 |
Теплоты гидратации некоторых соединений. [20] |
Это указывает на то, что теплоты гидратации соединений аддитивно слагаются из теплот гидратации образующих их ионов. [21]
Добавка кварцевого песка к цементу существенно влияет на гидролиз и гидратацию клинкерных соединений и способствует более полному использованию гидравлической активности вяжущего вещества. [22]
Теплоты гидратации отдельных ионов можно получить непосредственно из опытных значений теплот гидратации соединений, сделав определенные предположения о том, какую долю суммарной теплоты гидратации следует приписать каждому из ионов. Полученные таким методом величины теплот гидратации отдельных ионов называются экспериментальными, хотя все они являются в большей или меньшей степени произвольными и зависят от того, насколько близки к истине сделанные предположения. Их нельзя поэтому рассматривать как опытные, и их сравнение с вычисленными теплотами гидратации не дают возможности судить о степени совершенства того или иного теоретического метода. [23]
Теплоты гидратации отдельных ионов можно получить непосредственно из опытных значений теплот гидратации соединений, сделав определенные предположения о том, какую долю суммарной теплоты гидратации следует приписать каждому из ионов. Полученные таким методом величины теплот гидратации отдельных ионов называются экспериментальными, хотя все они являются в большей или меньшей степени произвольными и зависят от того, насколько близки к истине сделанные предположения. Их нельзя поэтому рассматривать как опытные, и их сравнение с вычисленными теплотами гидратации не дают возможности судить о степени совершенствования того или иного теоретического метода. [24]
Отработанная вода содержит также в растворенном виде имеющиеся в цементе или образующиеся при его гидратации соединения - гипс и гидрат окиси кальция. В неотработанной воде таких соединений содержится значительно меньше, вследствие чего она будет выщелачивать их из асбестоцементной массы, что приведет к нежелательному для производства ускорению схватывания и ряду других отрицательных явлений. [25]
В направлении изучения механизма и кинетики гидратации цементных соединений ведется дискуссия о том, как протекает гидратация цементных соединений - путем их растворения с последующей кристаллизацией гидратированных новообразований или путем непосредственного присоединения воды к твердому веществу ( по А. А. Байкову) с образованием коллоидных продуктов и последующей перекристаллизацией новообразований из мелких в более крупные вследствие их различной растворимости. [26]
Для каждого данного электролита сумма химических тешют или химических энергий гидратации ионов должна равняться сумме реальных теплот или реальных энергий гидратации тех же ионов и выражать суммарные теплоту или энергию гидратации соединения. Сопоставление данных табл. 12 с данными табл. 14 - 16 указывает на то, что это условие соблюдается недостаточно строго. Расхождение между теоретическими и опытными величинами объясняется главным образом тем, что различные авторы при проведении расчетов пользовались не одними и теми же исходными термохимическими данными. Результаты работ последнего времени обнаруживают лучшую сходимость. Это позволяет рассматривать теплоты гидратации АЯ и энергии гидратации AGft как достаточно надежные характеристики энергетического состояния ионов в водных растворах. [27]
Для каждого данного электролита сумма химических теплот или химических энергий гидратации ионов должна равняться сумме реальных теплот или реальных энергий гидратации тех же ионов и представлять собой суммарные теплоту или энергию гидратации соединения. Сопоставление данных табл. 11с данными табл. 17 - 19 указывает на то, что это условие соблюдается недостаточно строго. Расхождение между теоретическими и опытными величинами объясняется главным образом тем, что при проведении расчетов использовались не одни и те же исходные термохимические данные. Результаты работ последнего времени обнаруживают лучшую сходимость. Это позволяет рассматривать теплоты гидратации ДЯ /, и энергии гидратации ДОд как достаточно надежные характеристики энергетического состояния ионов в водных растворах. [28]
Влияние основных окислов СаО, SiO2 А12Оз на гидравлическую активность шлаков заключается в том, что СаО и особенно А12Оз повышают гидравлическую активность шлаков, a SiO2, имеющийся в избытке по отношению к глинозему и окиси кальция, тормозит процессы кристаллизации и гидратации соединений шлака, уменьшая тем самым их активность. [29]
Влияние основных окислов СаО, SiO2, А12Оз на гидравлическую активность шлаков заключается в том, что СаО и особенно А12Оз повышают гидравлическую активность шлаков, a SiO2, имеющийся в избытке по отношению к глинозему и окиси кальция, тормозит процессы кристаллизации и гидратации соединений шлака, уменьшая тем самым их активность. [30]
Страницы: 1 2 3