Гидратность
Cтраница 1
Гидратность соли не указана. [1]
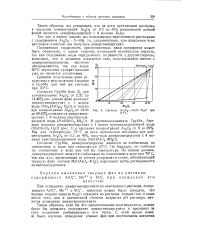 |
Система As2O. - МпО - Н2О при. [2] |
Пониженная гидратность приготовленных нами препаратов может быть объяснена, с одной стороны, возможной неточностью анализа, так как содержание воды определялось по разности, с другой стороны, возможно, что в условиях осаждения гипс, получающийся вместе с димарганецарсенатом, частично обезвоживается, так как выше 65 С двуводный сульфат кальция уже не является устойчивым. [3]
Степень гидратности ферроцианидов не указана; большинство солей - кристаллогидраты с различным содержанием воды. [4]
Степень гидратности солей не указана. [5]
 |
Частоты v ( CN и отрицательные логарифмы растворимости рс ферроцианидов х металлов. [6] |
Степень гидратности ферроцианидов не указана. [7]
 |
Колебательные частоты ( еле 1 некоторых ( по нашим данным. [8] |
Степень гидратности солей не указана. [9]
Данные о гидратности CdF2 противоречивы. Своеобразные явления, наблюдающиеся при попытках определения растворимости этого вещества, истолкованные Нука 22 ] как доказательство существования ряда его модификаций, вызваны, вероятно, медленным переходом кристаллов в устойчивую безводную фазу. [10]
Таким образом, гидратность солей существенно зависит от заряда, радиуса и типа электронной оболочки катиона. Тетрафторобо-раты прочих щелочных металлов, аммония и гидразония известны только в виде безводных солей. [11]
Аммонизированный суперфосфат при охлаждении схватывается, что объясняется изменением гидратности мономагнийфосфата и образованием других кристаллогидратов. [12]
Аммонизированный суперфосфат при охлаждении схватывается, что объясняется изменением гидратности мономагнийфос-фата и образованием других кристаллогидратов. [13]
Проведенными опытами уточнены условия кристаллизации MgNH4PO4 Н2О и MgNH4PO4 6 Н2О из чистых фосфорнокислых растворов и изучено влияние некоторых примесей на гидратность выделяющегося магнииаммонийфосфата. [14]
Полученная этими авторами изотерма состоит из ветвей насыщения трехводным димагнийфосфатом MgHPO4 ЗН2О и мономагнийфосфатом Mg ( H2PO4) 2 - xH2O, гидратность которого авторами не установлена. Камерон и Белл [4] отметили также, что фосфат магния, более основной, чем димагнийфосфат, существует при 25 в равновесии только с крайне разбавленными относительно Р2О5 растворами. Концентрации этих растворов слишком малы, чтобы их можно было определить сколько-нибудь точно. Как мы увидим далее, результаты Камерона и Белла являются достоверными лишь для ветви насыщения димагнийфосфата. [15]
Страницы: 1 2