Гидрид - медь
Cтраница 1
Гидрид меди, формула которого, по-видимому, должна быть СиН, является оригинальным соединением, аналогичных которому нет для других металлов. До недавнего времени это был единственный гидрид, синтез которого осуществляется из водных растворов. [1]
Гидрид меди бурно реагирует с соляной кислотой [595], полностью растворяется в концентрированном аммиаке и легко реагирует с окислителями в щелочной среде. [2]
Гидрид меди - красно-бурый порошок, очень легко окисляющийся на воздухе. [3]
Гидриды меди, серебра, золота, цинка, кадмия, ртути, индия и таллия отнесены Хердом к так называемым промежуточным гидридам, занимающим по своим свойствам место между ковалентными гидридами и гидридами переходных металлов. [4]
Гидрид меди, СиН, получают восстановлением сульфата меди фосфорноватистой кислотой Н6Р204 при нагревании. [5]
Гидрид меди представляет собой коричневые кристаллы с кубической гранецентрированнои решеткой; он медленно окисляется на воздухе ( на холоду) и выделяет водород при легком нагревании. [6]
Известен гидрид меди ( I) СиН - кристаллическое вещество красно-бурого цвета. [7]
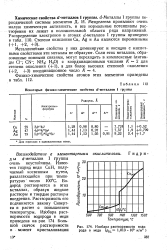 |
Изобара растворимости водорода в меди ( рНз 1 013 105 и / ж2. [8] |
Известен гидрид меди СиН, получаемый косвенным путем, разлагающийся при температурах4 около 100 С. Водород растворяется в этих металлах, образуя жидкие растворы и твердые растворы внедрения. Растворимость его подчиняется закону Сиверт-са и растет с повышением температуры. [9]
Известен гидрид меди ( I) СиН - кристаллическое вещество красно-бурого цвета. [10]
Реально существующий гидрид меди впервые был получен восстановлением солей меди гипофосфитом натрия в водном растворе. [11]
Существование гидрида меди ( CuHB) в гиде химического соединения не доказано - Возможно, что в действительности о пнлястся адсорбционной смесыо. [12]
Существование гидрида меди подтверждено синтезом его через обменные химические реакции; для золота и серебра таких реакций неизвестно. [13]
Свойствам гидрида меди, получаемого реакцией Вюрца, в настоящее время посвящено большое число работ, систематическое изложение которых приводится, например, у Гме-лина [ 6, № 60, стр. Однако интересно отметить некоторые свойства гидрида меди, связанные с практическим применением этого неустойчивого соединения. [14]
Авторы синтезировали гидрид меди [55] и показали, что он реагирует с алкилмедными соединениями, образуя углеводороды. [15]
Страницы: 1 2 3 4