Гидрид - металл
Cтраница 2
Гидриды металлов подгруппы ПА способны вступать в такие же реакции присоединения, как и гидриды щелочных металлов. Взаимодействие гидрида кальция с метилборатом, приводящее к образованию триметоксиборгидрида кальция, идет в узких температурных пределах - 210 - 230 С. [16]
Некоторые гидриды металлов, например TiH2, CuH, SnH4, РЬН4, вообще не вступают в реакции с водой. [17]
Если неустойчивые гидриды металлов считать промежуточными продуктами при гидрогенизации, то металлы, о которых идет речь, должны легко давать гидриды при обработке водородом. [18]
Среди гидридов металлов представляют определенный интерес гидриды бериллия, лития и их более сложные соединения с другими элементами. В топлииных парах с кислородом и фтором они дают больший энергетический эффект, чем исходные металлы. Гидрид бериллия до недавнего времени был известен либо в виде растворов в эфирах, с которыми он образует комплексные соединения, либо в виде твердых бесцветных полимеров, содержащих обычно небольшое количество растворителя. [19]
 |
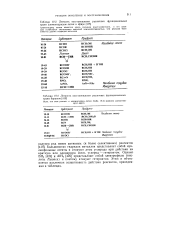
Содержание водорода в гидридах, имеющих наибольший потенциальный интерес для промышленного использования. [20] |
Среди гидридов металлов гидрид магния по крайней мере до 1960 г. был, вероятно, наиболее многообещающим для целей хранения водорода. Он содержит 7 65 % ( масс.) водорода, разлагается при относительно низких температуре и давлении ( 0 1 МПа при 560 К), причем давление остается постоянным практически для всей области ( от MgH2 до MgHo. Но этот гидрид труден в изготовлении прямым соединением элементов. Зависимость давления водорода от температуры для этого гидрида такова, что его можно практически использовать при температуре отходящего тепла около 670 К. Отработанного тепла двигателя внутреннего сгорания едва хватает для разложения гидрида. Кинетика образования гидрида магния улучшается при содержании в магнии 5 % никеля или меди. [21]
Присоединение гидрида металла к внутренним двойным связям происходит гораздо медленнее, чем к концевым. [22]
Из гидридов металлов, меченных тритием [2618], легко могут быть получены комплексные алюмогидриды, содержащие тритий. [23]
Технология гидридов металлов изучена еще недостаточно, и естественно, что методы получения их также мало известны. [24]
Присутствие гидридов металлов в сплавах повышает их хрупкость. [25]
 |
Легкость восстановления различных функциональных групп алюмогидридом лития в эфире.| Легкость восстановления различных функциональных групп бораном. [26] |
Большинство гидридов металлов представляет собой нук-леофильные агенты и атакуют атом углерода при действии на кратную или одинарную связь углерод - гетероатом. Однако ВН3 [424] и А1Н3 [425] представляют собой электрофилы ( кислоты Льюиса) и поэтому атакуют гетероатом. [27]
Присоединение гидридов металлов к олефиновым углеводородам широко исследовалось преимущественно на гидридах бора и алюминия. [28]
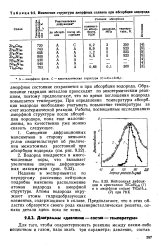 |
Изменение структуры аморфных сплавов при абсорбции водорода.| Нейтронная дифракция в кристаллах TiCuHo. gs ( 1 и в аморфном сплаве ( 2 при 78 К. [29] |
Образование гидридов металлов происходит по экзотермическим реакциям, поэтому предполагают, что во время поглощения водорода повышается температура. При определении температуры абсорбции водорода необходимо учитывать повышение температуры за счет экзотермической реакции. Работы, посвященные исследованию аморфной структуры после абсорбции вородора, яока еще малочисленны, но качественно уже можно оказать следующее. [30]
Страницы: 1 2 3 4