Гидрид - редкоземельный металл
Cтраница 1
Гидриды редкоземельных металлов получают восстановлением магния окислов редкоземельных металлов в токе водорода в закрытой системе при температуре, достаточной для восстановления. В специальной реторте смешивают 4 г прокаленной окиси редкоземельного металла с размерами частиц 60 меш. Помещают реторту в трубчатую печь и пропускают водород со скоростью 4 л / мин, нагревая одновременно печь. Выше 420е С водородное пламя в печи становится из бесцветного белым за счет насыщения частицами образующегося MgO. С током водорода через медную трубу MgO попадает ъ ловушку, помещенную в охлаждаюший раствор. [1]
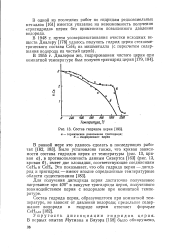 |
Состав гидридов церия. [2] |
В одной из последних работ по гидридам редкоземельных металлов [161] имеется указание на невозможность получения тригидрида церия без применения повышенного давления водорода. [3]
 |
Содержание водорода в электроосажденкых металлах. [4] |
Например, Винклер еще в конце прошлого столетия [69, 70] получал гидриды редкоземельных металлов, нагревая смесь их окислов и металлического магния в присутствии водорода. [5]
Однако пятидесятые годы вновь привели к широкому развитию работ по изучению гидридов редкоземельных металлов, главным образом церия, одновременно в ряде стран, в результате чего были получены новые интересные данные. [6]
Однако, как отмечалось в § 9, существуют фазы внедрения ( например, гидриды редкоземельных металлов), в которых внедренные атомы располагаются как на ок-таэдрических, так и на тетраэдрических междоузлиях. Поэтому представляет интерес рассмотреть диффузию внедренных атомов в том случае, когда диффузионный путь атома проходит через ряд чередующихся октаэдри-ческих и тетраэдрических междоузлий, в которых эти атомы имеют различную потенциальную энергию. [7]
При нагревании в вакууме выше 1000 гидриды полностью разлагаются. Гидриды редкоземельных металлов неустойчивы во влажном воздухе. Растворяются в кислотах с образованием соответствующих солей. [8]
Гидриды переходных металлов более инертны по отношению к воде и водным растворам кислот. Только гидриды редкоземельных металлов гидролизуются водой, остальные гидриды к воде н водяным парам относительно устойчивы. С кислотами гидриды металлов IV-VIII групп реагируют в очень жестких условиях - при большой концентрации кислоты и нагревании. Плавиковая кислота разлагает все гидриды. [9]
В вопросе выявления природы химической связи в гидридах переходных металлов решающее значение имеет анализ свойств водородных соединений элементов, находящихся в непосредственной близости с металлами, образующими со-леобразные гидриды. Особенный интерес приобретает изучение гидридов редкоземельных металлов и гидридов церия, в частности характеризующихся высокой абсорбцией водорода; они наиболее обстоятельно изучены к настоящему времени. О некоторой близости гидридов редкоземельных металлов к солеобразным гидридам свидетельствует уже их активная реакция с водой и характер изменения плотности: образование гидридов церия и лантана в противоположность ионным гидридам в общем сопровождается значительным уменьшением плотности ( табл. 13), но при переходе от дигидридов к тригидридам наблюдается небольшое повышение плотности. Гидриды европия и иттербия вообще образуются с увеличением плотности. Кроме того, Диалером [178] показано, например для церия, что уменьшение плотности этого металла при гидрировании, по сравнению с щелочными и щелочноземельными металлами, является скорее всего следствием малого изменения объема атома при ионизации. [10]
В вопросе выявления природы химической связи в гидридах переходных металлов решающее значение имеет анализ свойств водородных соединений элементов, находящихся в непосредственной близости с металлами, образующими со-леобразные гидриды. Особенный интерес приобретает изучение гидридов редкоземельных металлов и гидридов церия, в частности характеризующихся высокой абсорбцией водорода; они наиболее обстоятельно изучены к настоящему времени. О некоторой близости гидридов редкоземельных металлов к солеобразным гидридам свидетельствует уже их активная реакция с водой и характер изменения плотности: образование гидридов церия и лантана в противоположность ионным гидридам в общем сопровождается значительным уменьшением плотности ( табл. 13), но при переходе от дигидридов к тригидридам наблюдается небольшое повышение плотности. Гидриды европия и иттербия вообще образуются с увеличением плотности. Кроме того, Диалером [178] показано, например для церия, что уменьшение плотности этого металла при гидрировании, по сравнению с щелочными и щелочноземельными металлами, является скорее всего следствием малого изменения объема атома при ионизации. [11]
Наблюдается почти такая же картина взаимодействия, что и с металлами. Это подтверждает предположение о торможении образования селенидов в присутствии гидридов РЗМ. При 9 - ч обработке гидридов редкоземельных металлов H2Se также не было достигнуто разложения гидридов. Сумма лантана и селена всегда меньше 100 %, что свидетельствует о наличии водорода. Таким образом, верхняя корочка на металле представляет собой смесь гидрида с селенидом, а внутри находится гидрид редкоземельного металла. [12]
Наблюдается почти такая же картина взаимодействия, что и с металлами. Это подтверждает предположение о торможении образования селенидов в присутствии гидридов РЗМ. При 9 - ч обработке гидридов редкоземельных металлов H2Se также не было достигнуто разложения гидридов. Сумма лантана и селена всегда меньше 100 %, что свидетельствует о наличии водорода. Таким образом, верхняя корочка на металле представляет собой смесь гидрида с селенидом, а внутри находится гидрид редкоземельного металла. [13]
Страницы: 1