Гидрид - подгруппа
Cтраница 1
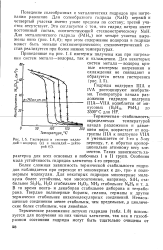 |
Гистерезис в системе палла. [1] |
Гидриды подгрупп III А и IVA диссоциируют необратимо. [2]
В гидридах подгруппы IIIA для бора и галлия х2; гидриды остальных элементов этой подгруппы представляют собой высокополимерные соединения. [3]
В гидридах подгруппы VIA для кислорода п 2, для серы п2 и 3, и более. [4]
Хотя в гидридах подгрупп IVA-VIIA основной связью является ковалентная, некоторый определенный вклад в общую энергию связи вносится также и ионной связью. [5]
Накопленные за последнее время данные о строении и свойствах гидридов подгруппы IIIA дозволяют выделить их в самостоятельный класс гидридов с водородной мостиковой связью. К этому классу относится и часть элементов подгруппы ПА, так как эти гидриды резко отличаются по строению и свойствам от ионных гидридов элементов подгрупп IA и ПА, граничащих с ними, а также от ковалентных гидридов соединений подгруппы IVA. Наличие водородных мостиков и электронного дефицита в атомах элементов указанных подгрупп делает эти гидриды способными к образованию комплексных гидридов, которые будут разобраны ниже, в то время, как гидриды элементов соседних подгрупп ПА и IVA не обладают такими свойствами. [6]
За исключением NHs, H20 и HF для всех гидридов подгрупп IVA, VIA и VILA характерно почти линейное повышение температур плавления и кипения с увеличением атомного веса элемента, образующего гидрид. Подобная закономерность наблюдается и для других соединений рассматриваемых элементов и инертных газов. [7]
Гидриды магния и бериллия, как правило, более активны, чем гидриды кальция, стронция и бария. Как и для гидридов подгруппы IA, для этих гидридов характерны реакции вытеснения водорода, передачи водорода другому элементу и присоединения. [8]
Водородные соединения щелочно-земельных металлов представляют собой твердые бесцветные нелетучие вещества с ярко выраженным солеббразным характером, как и гидриды щелочных металлов. Устойчивость гидридов повышается от Be к Са, а затем падает от Са к Ва. Гидриды подгруппы кальция могут быть получены прямым синтезом из элементов. [9]
 |
Энергия активации процесса самодиффузии водорода в гидридах переходных металлов. [10] |
Данные об электронной структуре гидридов можно также получить на основании исследования так называемых химических сдвигов в спектрах ЯМР гидридов переходных металлов. Эти сдвиги могут быть как положительными, так и отрицательными [119, 121 ], и для гидридов переходных металлов они часто значительно больше, чем для других химических соединений; это, несомненно, связано с металлическим характером гидридов. Можно предположить, что он будет примерно таким же для остальных гидридов подгруппы титана, несколько большим для гидридов подгруппы ванадия и меньшим ( или даже отрицательным) для гидридов металлов III группы. [11]
 |
Энергия активации процесса самодиффузии водорода в гидридах переходных металлов. [12] |
Данные об электронной структуре гидридов можно также получить на основании исследования так называемых химических сдвигов в спектрах ЯМР гидридов переходных металлов. Эти сдвиги могут быть как положительными, так и отрицательными [119, 121], и для гидридов переходных металлов они часто значительно больше, чем для других химических соединений; это, несомненно, связано с металлическим характером гидридов. Можно предположить, что он будет примерно таким же для остальных гидридов подгруппы титана, несколько большим для гидридов подгруппы ванадия и меньшим ( или даже отрицательным) для гидридов металлов III группы. [13]
Отчетливой границы между указанными группами нет, имеются элементы с промежуточным типом связи. В какой-то степени этн свойства предполагаются у гидридов нттрня и актннондов. Гндрнд магния является промежуточным между соединениями с ионными и ковалентными связями. Гидриды подгрупп бора н цинка представляют собой полимерные соединения с ковалентным типом связи, а соединения подгруппы медн с водородом - типичные переходные соединения от металлических к ковалентным. I - IIIВ подгрупп выделяют в отдельную группу, основным признаком которой авторы считают существование водородных мостиковых связей. Последние служат причиной образования днмеров молекул этих соединений. Однако, по мнению авторов, эта группа является переходной между ковалентными и металлическими водородными соединениями. [14]
Страницы: 1