Гидрид - рубидий
Cтраница 1
Гидриды рубидия и цезия менее известны. Вероятно, и у этих гидридов наблюдается увеличение скорости образования из элементов с увеличением атомного номера. [1]
Гидриды рубидия и цезия чрезвычайно химически активные соединения. Они разлагают воду ( бурно) и этанол, выделяя водород и образуя соответственно гидроокиси и алкоголяты. При нагревании с азотом и аммиаком образуют амиды, с фосфором - фосфиды, с ацетиленом - ацетилиды. [2]
Гидриды рубидия и цезия синтезируют в установке, используемой для получения гидрида лития синтетическим методом ( см. стр. В установке создают вакуум и цилиндр 4 с лодочкой 3 медленно нагревают до 620 С. [3]
 |
Диаграмма состояния системы КН - КОН. [4] |
Гидрид рубидия растворяется в расплавленных солях, а также в расплавленном металлическом рубидии. [5]
Гидриды рубидия и цезия чрезвычайно химически активные соединения. Они разлагают воду ( бурно) и этанол, выделяя водород и образуя соответственно гидроокиси и алкоголяты. Уже под действием паров воды воздуха МеН окисляются, воспламеняясь. При нагревании с азотом и аммиаком образуют амиды, с фосфором - фосфиды, с ацетиленом - ацетилиды. [6]
Гидриды рубидия и цезия разлагают воду и спирт, выделяя водород и образуя соответственно гидроокиси или алкоголяты. [7]
Гидрид рубидия менее устойчив, чем гидрид натрия; водород в RbH электроотрицателен. [8]
Гидриды рубидия еще менее устойчивы, чем аналогичные соединения калия ли натрия. Соединение RbH образуется с выделением 12 ккал / моль. Астахову [27], RbH относится к соединениям, обладающим ионной связью. [9]
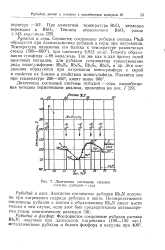 |
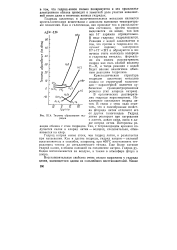
Диаграмма состояния сплавов системы рубидий - сера. [10] |
Азотистое соединение рубидия Rb3N получено при нагревании гидрида рубидия в аеоте. [11]
При пропускании сухого водорода над слегка нагретым рубидием образуется гидрид рубидия RbH с кристаллической решеткой типа NaCl, имеющий период а0 6037 нм; рентгеновская плотность р2 59 Мг / м3; теплота образования этого соединения ДЯ0бр54 98 кДж / моль. [12]
Упругость пара гидридов достигает атмосферного давления при сравнительно низких температурах - при 364 С в случае гидрида рубидия и 389 С в случае гидрида цезия. [13]
Химическая активность ионных гидридов растет в том же направлении, что и активность соответствующих металлов - от легких элементов к тяжелым. Гидриды рубидия и цезия даже воспламеняются во влажном воздухе; гидриды щелочноземельных металлов несколько менее активны, чем гидриды щелочных металлов. [14]
 |
А. Теплоты образования гидридов. [15] |
Страницы: 1 2