Гидрид - углерод
Cтраница 1
Гидриды углерода, или углеводороды, имеют молекулы с углеродным остовом, образующим неразветвленные или разветвленные цепи либо циклические структуры. Чем отличается строение углеводородов и гидридов бора. [1]
Гидриды углерода, углеводороды, широко распространены в природе. Гидридов бора в природе нет, а первые же синтезированные гидриды, например диборан, были крайне неустойчивыми, поэтому казалось, что химия бороводородов будет чрезвычайно ограниченной. Однако сейчас известно уже около 30 - 50 гидридов бора, а если считать изомеры и продукты замещения, их уже несколько сотен. Более того, многие из этих соединений термически стабильны и некоторые даже более устойчивы, чем известные органические соединения. Химия бороводородов только начинает свое развитие и, возможно, со временем будет соперничать с химией углеводородов. [2]
Гидриды углерода ( углеводороды) подробно рассматриваются в курсах органической химии. Настоящий раздел посвящен только химии гидридов кремния и германия. [3]
 |
Термодинамические характеристики реакций образования гидридов некоторых элементов. [4] |
Гидриды углерода, азота и других элементов IV и V групп получают просто взаимодействием солей анионов этих элементов с водой, как описано в разд. Скорость гидролиза таких солей обычно возрастает в кислых растворах, где имеется больше протонов, доступных для анионов, и где, согласно принципу Ле Шателье, основной продукт удаляется или нейтрализуется кислотой. [5]
Гидриды углерода СН, С2Н4, С2Н2, СбН, СвН и др. называются углеводородами. [6]
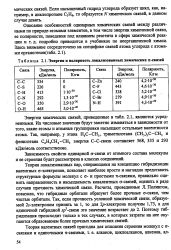 |
Энергия и полярность локализованных химических а-связей. [7] |
Если насыщенный гидрид углерода образует цикл, как, например, в циклопропане С3Н6, то образуется N химических связей, в данном случае девять. [8]
Все сказанное свидетельствует о заметных и еще мало понятных проявлениях индивидуальности в свойствах ненасыщенных фторидов и гидридов углерода и кремния. [9]
Не вызывает сомнения, что те исключительные свойства, которые определяют единственный в своем роде характер органических соединений, принадлежат исключительно не углероду или водороду, а соединениям, образованным этими двумя элементами, - гидридам углерода, или углеводородам. Теоретически и в еще большей степени практически все органические соединения можно считать производными углеводородов, получающимися при замещении атомов водорода атомами других элементов. Углеводороды образуют естественную основу классификации всех органических соединений. Отсюда вытекает ясное определение, лучше всего отражающее действительность: органическая химия - это химия углеводородов и их производных ( К. [10]
Не вызывает сомнения, что те исключительные свойства, которые определяют единственный в своем роде характер органических соединений, принадлежат исключительно не углероду пли водороду, а соединениям, образованным этими двумя элементами, - гидридам углерода, или углеводородам. Теоретически и в ещ большей степени практически все органические соединения можно считать производными углеводородов, получающимися при замещении атомов водорода атомами других элементов. Углеводороды образуют естественную основу классификации всех органических соединении. Отсюда вытекает ясное определение, лучше всего отражающее действительность: органическая химия - это химия углеводородов и их производных ( К. [11]
Органические соединения, а точнее углеводороды, имеют принципиальные отличия в сравнении с неорганическими соединениями такими, как кислоты и основания, оксиды и соли и даже по сравнению с неорганическими гидридами - Н2О, NH3, SiH, HF, H2S, AsH3 и др. Эти принципиальные особенности органических молекул ( как правило, гидридов углерода и углеводородных остатков функциональных произведемте углеводородов) суммированы на схеме В. [12]
Наблюдающаяся высокая химическая активность радикалов обусловлена незаполненностью их электронных оболочек. Характерна аналогия между химическими свойствами гидридов углерода, азота, кислорода и фтора и химическими свойствами атомов с тем же числом электронов. Так, радикал СН ( метин) является химическим аналогом атома N, радикалы СН2 ( метилен) и NH ( имин) - аналогами атома О, радикалы СН3 ( метил), NH2 ( аминогруппа) и ОН ( гидроксил) - аналогами атома F и, наконец, молекулы СН4, NH3, Н20 и HF в известном смысле ( инертность) аналогичны атому Ne. Благодаря химической ненасыщенности радикалов энергия активации процессов, протекающих с их участием, имеет порядок величины энергии активации атомных реакций. Поэтому такие процессы, как правило, идут приблизительно с такой же скоростью, с какой идут атомные процессы. [13]
Все оксиды углерода СО, СО2, С3О2, С6О6 и их производные изучает неорганическая химия. Следовательно, в органической химии остаются гидриды углерода - углеводороды и все их функциональные производные. [14]
Наблюдающаяся высокая химическая активность радикалов обусловлена незаконченностью электронных оболочек соответствующих атомных групп, благодаря чему свойства этих групп приближаются к свойствам атомов, обладающих тем же количеством внешних электронов, что и данная атомная группа. В этом отношении характерна аналогия между химическими свойствами гидридов углерода, азота, кислорода и фтора и химическими свойствами атомов с тем же числом электронов. Так, радикал СН ( метин) является химическим аналогом атома N, радикалы СН2 ( метилен) и NH ( имин) - аналогами атома О, радикалы СН3 ( метил), NHa. ОН ( гидроксил) - аналогами атома F и, наконец, молекулы СН4, NH3, Н8О и HF в известном смысле ( инертность) аналогичны атому Ne. Благодаря химической ненасыщенности радикалов энергия активации процессов, протекающих с их участием, имеет порядок величины энергии активации атомных реакций. Поэтому эти процессы, как правило, идут приблизительно с такой же скоростью, с какой идут атомные процессы. [15]
Страницы: 1 2