Гидрид - цезий
Cтраница 1
Гидрид цезия растворяется в расплавленных солях и расплавленном металлическом цезии. [1]
Гидрид цезия, CsH, образуется в результате взаимодействия исходных элементов при 400; его получают также нагреванием окисла Cs20 при 150 в токе водорода. Гидрид представляет собой белые кубические кристаллы с плотностью 3 67 г / см3 ( решетка типа NaCl, межионное расстояние 3 19 А); он менее устойчив, чем гидриды остальных щелочных металлов. [2]
Гидрид цезия CsH получают реакцией между цезием и чистым водородом. При образовании кристаллов CsH выделяется 12 ккал / моль теплоты. Астахову [27], CsH относится к соединениям с ионной связью. [3]
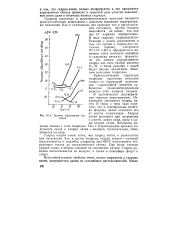 |
А. Теплоты образования гидридов. [4] |
Восстановительные свойства очень сильно выражены у гидрида цезия, являющегося одним из сильнейших восстановителей. [5]
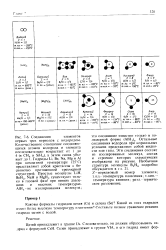 |
Соединения элементов. [6] |
Какой из этих гидридов имеет более высокую температуру плавпения Составьте полное уравнение реакции гидрида цезия с водой. [7]
Упругость пара гидридов достигает атмосферного давления при сравнительно низких температурах - при 364 С в случае гидрида рубидия и 389 С в случае гидрида цезия. [8]
Гидрид цезия - чрезвычайно химически активное вещество, воспламеняется на воздухе, содержащем следы влаги, а также в среде хлора и фтора, при нагревании диссоциирует с образованием водорода и цезия. Давление паров диссоциации достигает атмосферного при 304 С. [9]
На основе справочных данных сравните окислительные и восстановительные свойства водорода и простых веществ: а) цезия, б) алюминия, в) золота, г) хлора, д) азота. Укажите, в чем заключается сходство и различие между веществами: а) гидрид алюминия и гидрид цезия, б) хлорид цезия и аурид цезия, в) хлорид золота ( III) и хлороводород, г) нитрид цезия и нитрид трихлора, д) нитрид алюминия и аммиак. [10]
Гидриды щелочных металлов являются очень ре-акционноспособными веществами. Хотя и указывают, что при равных степенях дисперсности гидридов и соответствующих металлов первые менее активны, на практике, в большинстве случаев, тонкие порошки или пористые массы гидридов реагируют более энергично, чем компактные металлы. По химическим свойствам все гидриды щелочных металлов очень похожи друг на друга, но реакционная активность увеличивается от гидрида лития к гидриду цезия. Реакционная способность гидридов в известной степени зависит от растворимости продуктов реакции в реакционной среде. [11]
В ряду щелочных металлов восстановительная способность гидридов увеличивается с ростом атомного веса металла. В гидриде лития связь Li - Н имеет частично ковалентный характер, на что указывает некоторая растворимость в полярных органических растворителях, а также то, что во влажном воздухе гидркд лития разлагается лишь медленно. Гидрид цезия - активный восстановитель уже при комнатной температуре, на воздухе он самовоспламеняется. [12]
Страницы: 1